题目内容
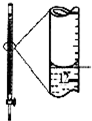
10.下列有关实验的装置、试剂选用或操作正确的是( )| A.配制0.10mol•L-1溶液 | B.除去CO中的CO2 | C.苯萃取碘水中I2,分出水层后的操作 | D.记录滴定终点读数为12.20mL |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
分析 A.容量瓶只能配制溶液,不能稀释或溶解药品;
B.洗气除杂时,要除去杂质但不能引进新的杂质,且导气管遵循“长进短出”原则;
C.萃取时,苯密度小于水密度,所以苯在水的上层;
D.滴定管中大刻度在下边,小刻度在上边.
解答 解:A.容量瓶只能配制溶液,不能稀释或溶解药品,所以溶解烧碱时不能用容量瓶,应该用烧杯,故A错误;
B.洗气除杂时,要除去杂质但不能引进新的杂质,且导气管遵循“长进短出”原则,该装置符合条件,故B正确;
C.萃取时,苯密度小于水密度,所以苯在水的上层,所以含有碘的苯层应该从上口倒出,故C错误;
D.滴定管中大刻度在下边,小刻度在上边,记录滴定终点读数为11.80mL,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及仪器的使用、基本操作、除杂等知识点,明确仪器使用方法、基本操作规范性是解本题关键,注意滴定管和量筒刻度区别,题目难度不大.

练习册系列答案
相关题目
4.某物质属于电解质,则该物质不可能属于( )
| A. | 金属氧化物 | B. | 强碱 | C. | 单质 | D. | 正盐 |
18.设阿伏加德罗常数为NA,则下列说法正确的是( )
| A. | 常温常压下,11.2 L甲烷中含有的氢原子数为2NA | |
| B. | 标准状况下,0.3 mol二氧化硫中含有的氧原子数为0.3NA | |
| C. | 常温常压下,2 g H2的分子数为NA | |
| D. | 常温常压下,1 mol/L MgCl2溶液中含Cl-数为2NA |
5.已知反应:
①101kPa时,C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1=-110.5kJ•mol-1
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ•mol-1
下列结论正确的是( )
①101kPa时,C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1=-110.5kJ•mol-1
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ•mol-1
下列结论正确的是( )
| A. | 浓硫酸与稀NaOH溶液反应的中和热为57.3 kJ•mol-1 | |
| B. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出的热量为57.3 kJ | |
| C. | 若碳的燃烧热用△H3来表示,则△H3<△H1 | |
| D. | 若碳的燃烧热用△H3来表示,则△H3>△H1 |
15.下列说法中正确的是( )
| A. | 可以用KSCN溶液检验${\;}_{26}^{45}$FeCl3和${\;}_{26}^{56}$FeCl3 | |
| B. | H2O与D2O互称同素异形体 | |
| C. | 副族元素中没有非金属元素,所以又称过渡金属 | |
| D. | F-与K两种微粒之间可以形成离子键 |
2.下列反应中的氨与反应4NH3+5O2→4NO+6H2O中的氨作用相同的是( )
| A. | 2Na+2NH3→2NaNH2+H2↑ | B. | NH3+HNO3→NH4NO3 | ||
| C. | 4NH3+6NO→5N2+6H2O | D. | 3SiH4+4NH3→Si3N4+12H2 |
19.生活中的一些问题常涉及到化学知识,则下列叙述正确的是( )
| A. | 高温能杀死流感病毒是因为构成病毒的蛋白质受热变性 | |
| B. | 明矾和漂白粉常用于自来水的处理,两者的作用原理相同 | |
| C. | 氯化铁溶液可用于制作印刷电路板是因为其具有较强氧化性,与铜发生置换反应 | |
| D. | 晶体硅具有半导体的性质,所以可以制作光导纤维 |
20.取m g相对原子质量为M的某金属与足量稀硫酸反应,在标准状况下产生a L氢气,该反应生成的硫酸盐中金属的化合价为( )
| A. | +$\frac{aM}{11.2m}$ | B. | +$\frac{am}{11.2M}$ | C. | +$\frac{11,2m}{aM}$ | D. | +$\frac{aM}{22.4m}$ |