题目内容
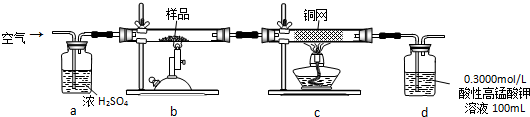
10.某同学用下图所示装置制取溴苯和溴乙烷.已知:(CH3CH2OH+HBr-CH3CH2Br+H2O)溴乙烷为无色液体,难溶于水,沸点为38.4℃,熔点为-119℃.
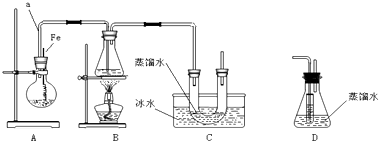
主要实验步骤如下:
①组装好装置,检查其气密性.
②向烧瓶中加入一定量苯和液溴,向锥形瓶中加入乙醇至稍高于进气导管口处,向U型管中加入蒸馏水封住管底,向水槽中加入冰水.
③将A装置中的纯铁丝小心向下插入苯和液溴的混合液中.
④点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10分钟.
请填写下列空白:
(1)请写出A装置中所发生的有机反应化学方程式A:
 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$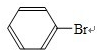 +HBr
+HBr(2)简述步骤①检验装置气密性的具体做法(不包括D)组装好装置后,在U型右边导管口连接一个管带有胶管的玻璃导管,将导管放入水面下,加热烧瓶,若导管口处有气泡产生,停止加热后导管内有一段水柱产生,证明装置的气密性良好
(3)C装置中U型管内部用蒸馏水封住管底的作用是溶解吸收溴化氢气体,防止溴化氢及产物逸出污染环境
(4)反应完毕后,U型管内液体分层,溴乙烷在下(填:上或下)层.
(5)为证明溴和苯的上述反应是取代反应而不是加成反应,该学生用装置D代替装置B、C直接与A相连重新操作实验.
①装置D的锥形瓶中,小试管内的液体是苯(或四氯化碳)(任填一种符合题意试剂的名称),其主要作用是吸收挥发出来的溴蒸气.
②反应后向锥形瓶中滴加硝酸银溶液(或紫色石蕊试液)(任填一种符合题意试剂的名称),若有淡黄色沉淀产生(或紫色石蕊试液变红)证明该反应为取代反应.
(6)要检验某溴乙烷中的溴元素,正确的实验方法是D
A.加入新制的氯水振荡,再加入少量CCl4振荡,观察下层是否变为橙红色
B.滴入硝酸银溶液,再加入稀硝酸使溶液呈酸性,观察有无浅黄色沉淀生成
C.加入NaOH溶液共热,冷却后加入硝酸银溶液,观察有无浅黄色沉淀生成
D.加入NaOH溶液共热,冷却后加入稀硝酸使溶液呈酸性,再滴入硝酸银溶液,观察有无浅黄色沉淀生成.
分析 (1)苯在铁做催化剂时可以和溴发生取代反应获得溴苯;
(2)根据压强差产生气泡判断装置气密性;
(3)氢溴酸是强酸,水可以阻止物质的溢出,起到水封的作用;
(4)溴乙烷的密度大于水;
(5)由图可知,A中发生 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr,装置D的锥形瓶中小试管内苯(或四氯化碳)吸收溴,锥形瓶内的液体为水,吸收HBr气体,然后滴加硝酸银检验溴离子;
+HBr,装置D的锥形瓶中小试管内苯(或四氯化碳)吸收溴,锥形瓶内的液体为水,吸收HBr气体,然后滴加硝酸银检验溴离子;
(6)检验某溴乙烷中的溴元素,可以将溴乙烷碱性水解,再将溶液调成酸性,再检验溴离子即可;
解答 解:(1)苯在铁做催化剂时可以和溴发生取代反应获得溴苯,发生反应的原理方程式为: +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr,
+HBr,
故答案为: +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr;
+HBr;
(2)步骤①中检验装置气密性的具体做法是组装好装置后,在U型右边导管口连接一个管带有胶管的玻璃导管,将导管放入水面下,加热烧瓶,若导管口处有气泡产生,停止加热后导管内有一段水柱产生,证明装置的气密性良好,
故答案为:组装好装置后,在U型右边导管口连接一个管带有胶管的玻璃导管,将导管放入水面下,加热烧瓶,若导管口处有气泡产生,停止加热后导管内有一段水柱产生,证明装置的气密性良好;
(3)溴化氢极易溶于水,形成的氢溴酸是强酸,水可以阻止易挥发物质HBr的溢出,起到水封的作用,
故答案为:溶解吸收溴化氢气体,防止溴化氢及产物逸出污染环境;
(4)溴乙烷的密度大于水,所以反应完毕后,U型管内液体分层,溴乙烷在下层,
故答案为:下;
若发生加反应不生成副产物,若发生取代反应生成HBr,
(5)由图可知,A中发生 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$ +HBr,装置D的锥形瓶中小试管内苯(或四氯化碳)吸收溴,锥形瓶内的液体为水,吸收HBr气体,然后滴加硝酸银检验溴离子,所以①装置D的锥形瓶中,小试管内的液体是 CCl4,其主要作用是吸收挥发出来的溴蒸气,②反应后向锥形瓶中滴加 硝酸银溶液(或紫色石蕊试液),若 硝酸银溶液(或紫色石蕊试液)证明该反应为取代反应,
+HBr,装置D的锥形瓶中小试管内苯(或四氯化碳)吸收溴,锥形瓶内的液体为水,吸收HBr气体,然后滴加硝酸银检验溴离子,所以①装置D的锥形瓶中,小试管内的液体是 CCl4,其主要作用是吸收挥发出来的溴蒸气,②反应后向锥形瓶中滴加 硝酸银溶液(或紫色石蕊试液),若 硝酸银溶液(或紫色石蕊试液)证明该反应为取代反应,
故答案为:苯(或四氯化碳);吸收挥发出来的溴蒸气;硝酸银溶液(或紫色石蕊试液);有淡黄色沉淀产生(或紫色石蕊试液变红);
(6)检验某溴乙烷中的溴元素,可以将溴乙烷碱性水解,再将溶液调成酸性,再检验溴离子即可,其操作为加入NaOH溶液共热,冷却后加入稀硝酸使溶液呈酸性,再滴入硝酸银溶液,观察有无浅黄色沉淀生成,
故选D.
点评 本题考查了溴苯和溴乙烷的制取,这是一个综合性较强的实验题,连续制备两种产品溴苯和溴乙烷,需要根据题意及装置图示,联系所学知识合理分析完成,本题难度中等.


| 熔点 | 沸点 | |
| PCl3 | -112℃ | 75℃ |
| PCl5 | 148℃ | 200℃ |
(2)若发现C中气泡产生过猛,需要进行的操作的关键是用分液漏斗控制滴加液体的量或滴加速率.
(3)前期P过量生成三氯化磷,后期氯气过量生成五氯化磷,从PCl3和PCl5的混合物中分离出PCl3的最佳方法是a(选填序号).
a.蒸馏 b.分液 c.升华
(4)生成的PCl3在G中收集,则F中盛有冷水,作用是使得三氯化磷液化.
(5)C、D、H所盛的试剂分别是:C饱和食盐水;D浓硫酸;H碱石灰.
(6)如果E中反应放热较多,G处的导管可能发生堵塞,其原因是五氯化磷蒸汽冷却后变成固体.
| A. | 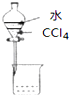 分离水和CCl4 | B. | 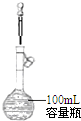 定容 | ||
| C. | 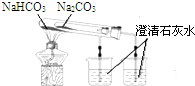 比较两种盐的热稳定性 | D. | 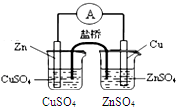 构成铜锌原电池 |
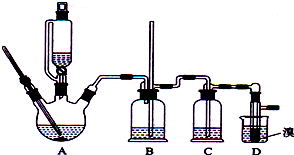 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2,CH2=CH2+Br2→BrCH2CHBr
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
(1)实验中制得的1,2-二溴乙烷的产量比理论值低的原因可能是A中反应温度没有迅速升高到170℃,部分乙醇生成了乙醚;A中反应温度过高,乙醇被浓硫酸氧化,生成乙烯的物质的量偏少;A中反应反应速率过快,导致乙烯通入的流速过快反应不充分.(至少写出两种)
(2)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去;
(3)若产物中有少量未反应的Br2,最好用d洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.饱和碳酸钠溶液
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”);依据是1,2-二溴乙烷的密度大于水
(5)若产物中有少量副产物乙醚.可用蒸馏的方法除去,理由是1,2-二溴乙烷的沸点132℃大于乙醚的沸点34.6℃,乙醚以气态被分离出去
(6)装置D若使用冰水冷却,则B中的主要现象是玻璃导管中的液面会升高,甚至溢出.
(7)请指出该实验装置的一处不足的地方缺乏尾气处理装置.
| A. | 若甲乙两容器均为恒容容器,则x必等于2 | |
| B. | 若甲乙两容器均为恒压容器,则x必等于3 | |
| C. | 若甲为恒压容器,乙为恒容容器,且x不等于3,则n1必大于n2 | |
| D. | 若甲为恒容容器,乙为恒压容器,且x等于3,则n1必大于n2 |