题目内容
19.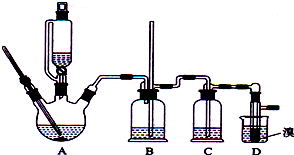 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2,CH2=CH2+Br2→BrCH2CHBr
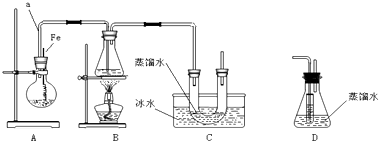
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
(1)实验中制得的1,2-二溴乙烷的产量比理论值低的原因可能是A中反应温度没有迅速升高到170℃,部分乙醇生成了乙醚;A中反应温度过高,乙醇被浓硫酸氧化,生成乙烯的物质的量偏少;A中反应反应速率过快,导致乙烯通入的流速过快反应不充分.(至少写出两种)
(2)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去;
(3)若产物中有少量未反应的Br2,最好用d洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.饱和碳酸钠溶液
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”);依据是1,2-二溴乙烷的密度大于水
(5)若产物中有少量副产物乙醚.可用蒸馏的方法除去,理由是1,2-二溴乙烷的沸点132℃大于乙醚的沸点34.6℃,乙醚以气态被分离出去
(6)装置D若使用冰水冷却,则B中的主要现象是玻璃导管中的液面会升高,甚至溢出.
(7)请指出该实验装置的一处不足的地方缺乏尾气处理装置.
分析 (1)乙醇在浓硫酸140℃的作用下发生分子间脱水生成乙醚,同时反应温度过高,乙醇被浓硫酸氧化,乙烯通入的流速过快反应不充分都会导致1,2-二溴乙烷的产量比理论值低;
(2)乙烯和溴水发生了加成反应,溴水会褪色;
(3)1,2-二溴乙烷在氢氧化钠溶液中可能水解,碳酸钠溶液呈碱性,也可以吸收Br2,据此答题;
(4)根据1,2-二溴乙烷和水的密度相对大小解答;
(5)利用1,2-二溴乙烷与乙醚的沸点不同进行解答;
(6)装置D若使用冰水冷却,1,2-二溴乙烷变成固态,会导致导管堵塞;
(7)根据实验装置图可知,实验中有少量的未反应的溴会污染空气,要有尾气吸收装置.
解答 解:(1)乙醇在浓硫酸140℃的作用下发生分子间脱水生成乙醚,同时反应温度过高,乙醇被浓硫酸氧化,乙烯通入的流速过快反应不充分都会导致1,2-二溴乙烷的产量比理论值低,
故答案为:A中反应温度没有迅速升高到170℃,部分乙醇生成了乙醚; A中反应温度过高,乙醇被浓硫酸氧化,生成乙烯的物质的量偏少;A中反应反应速率过快,导致乙烯通入的流速过快反应不充分;
(2)乙烯和溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷为无色,所以当溴的颜色完全褪去时,说明反应已经结束,
故答案为:溴的颜色完全褪去;
(3)1,2-二溴乙烷在氢氧化钠溶液中可能水解,碳酸钠溶液呈碱性,也可以吸收Br2,所以可以用饱和碳酸钠溶液洗涤,
故答案为:d;
(4)1,2-二溴乙烷和水不互溶,1,2-二溴乙烷密度比水大,
故答案为:下;1,2-二溴乙烷的密度大于水;
(5)1,2-二溴乙烷与乙醚的沸点不同,两者均为有机物,互溶,用蒸馏的方法将它们分离时,1,2-二溴乙烷的沸点132℃大于乙醚的沸点34.6℃,乙醚以气态被分离出去,
故答案为:1,2-二溴乙烷的沸点132℃大于乙醚的沸点34.6℃,乙醚以气态被分离出去;
(6)装置D若使用冰水冷却,1,2-二溴乙烷变成固态,会导致导管堵塞,此时装置B中玻璃导管中的液面会升高,甚至溢出,
故答案为:玻璃导管中的液面会升高,甚至溢出;
(7)根据实验装置图可知,实验中有少量的未反应的溴会污染空气,要有尾气吸收装置,而本实验中没有,
故答案为:缺乏尾气处理装置.
点评 该题较为综合,主要考查了乙醇制备1,2-二溴乙烷,掌握相关物质的基本化学性质,是解答本题的关键,平时须注意积累相关反应知识,难度中等.

 名校课堂系列答案
名校课堂系列答案已知:
 $→_{85℃}^{浓H_{2}SO_{4}}$
$→_{85℃}^{浓H_{2}SO_{4}}$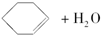

| 密度(g•cm-3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.
①A中碎瓷片的作用是防止液体暴沸,②导管B除了导气外还具有的作用是冷凝.
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水,振荡、静置、分层,分液后用c(填入编号)洗涤.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按如图2装置蒸馏,冷却水从g(填g或f)口进入.蒸馏时要加入生石灰,目的是除去环己烯中少量的水.
③收集产品时,控制的温度应在83℃左右,实验制得的环己烯精品质量低于理论产量,可能的原因是c.
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出.
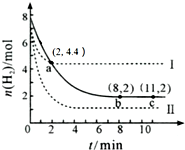
| A. | 该温度下,a点时,3 v正(CO2)=v正(H2) | |
| B. | 曲线Ⅱ对应的条件改变可能是充入氦气 | |
| C. | 曲线Ⅰ对应的条件改变可能是降低温度 | |
| D. | 从反应开始至a点,v (CO2)=0.6 mol•L-1•min-1 |
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A. | 反应在前5s的平均速率v(A)=0.17mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(A)=0.41mol•L-1,则反应的△H>0 | |
| C. | 相同温度下,起始时向容器中充入2.0mol C,达到平衡时,C的转化率大于80% | |
| D. | 相同温度下,起始时向容器中充入0.20mol A、0.20mol B和1.0mol C,反应达到平衡前v(正)<v(逆) |
| A. | 容器内压强不再随时间变化 | |
| B. | 混合气体的颜色不再改变 | |
| C. | I2与H2在混合气体中的体积分数相等 | |
| D. | H2、I2、HI的浓度相等 |
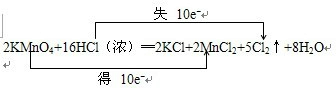 .
.
 +Br2$\stackrel{Fe}{→}$
+Br2$\stackrel{Fe}{→}$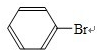 +HBr
+HBr