题目内容
4.寻找新能源是解决温室效应的一条重要思路.磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li $?_{充电}^{放电}$ LiFePO4,电池中的固体电解质可传导离子,下列说法错误的是( )| A. | 放电时正极材料是磷酸亚铁锂(LiFePO4) | |
| B. | 放电时正极反应为:FePO4+Li++e-═LiFePO4 | |
| C. | 充电时Li+和Fe2+向阴极移动,PO43ˉ向阳极移动 | |
| D. | 充电时阴极反应为:Li++e-═Li |
分析 根据电池反应可知,放电时LiFePO4电池负极反应为Li-e-═Li+,正极反应为FePO4+Li++e-═LiFePO4;充电时的阳极反应和原电池中正极反应相反,阴极反应和原电池中负极反应相反,根据原电池和电解池的工作原理来回答.
解答 解:A.反应中Li被氧化,应为原电池的负极,Fe元素化合价降低,被还原,则FePO4为正极,故A错误;
B.放电时正极发生还原反应,正极反应为FePO4+Li++e-═LiFePO4,故B正确;
C.充电时,Li+向阴极移动,被还原生成Li,FePO4-向阳极移动,被氧化生成FePO4,故C错误;
D.由电池总方程式可知充电时阴极反应为:Li++e-═Li,故D正确.
故选AC.
点评 本题考查化学电源新型电池知识,本题难度不大,注意根据电池反应书写电极反应式的方法,以及离子的定向移动问题.

练习册系列答案
相关题目
12.类推的思维方法可解决不少化学问题,但类推的结论最终要经过实践的检验才能确定其正确与否.下列几种类推结论中,你认为正确的是( )
| A. | 沸点HBr>HCl,则同族元素氢化物沸点HCl>HF | |
| B. | Fe3O4可表示为FeO•Fe2O3,则Pb3O4可表示为PbO•Pb2O3 | |
| C. | CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应也只生成Na2SO3和O2 | |
| D. | SiO2能形成原子晶体,一定条件下CO2也能形成原子晶体 |
19.下列说法正确的是( )
| A. | 右列图标均与燃烧和爆炸有关 | |
| B. | 棉、麻、蚕丝、羊毛及合成纤维都属于纤维,但均不含纤维素 | |
| C. | 科学家用单个分子制成了“纳米车”,它能在人工操纵下运输药物分子到病源处释放以杀死癌细胞.“纳米车”说明在一定条件下,分子的热运动须在人工操纵下才能进行 | |
| D. | 捕获工业排放的CO2,既能降低地球的温室效应又能用来合成聚碳酸酯可降解塑料,实现碳的循环利用 |
16.甲、乙是由短周期元素组成的常见物质或微粒,在中学化学中有许多物质或微粒能满足下列相互转化关系:甲$\stackrel{H+}{→}$乙$\stackrel{OH-}{→}$甲.下列说法正确的是( )
| A. | 甲有可能是AlO2- 也有可能是Al3+ | |
| B. | 若乙为无色无味气体,则甲一定是CO32- | |
| C. | 若甲是具有刺激性气味的气体,则甲、乙具有相同的电子数 | |
| D. | 若甲、乙均为离子,甲、乙两种离子在同一溶液中一定不能大量共存 |
13.溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )
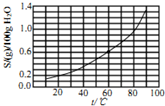

| A. | 25℃时,溴酸银微溶于水 | |
| B. | 溴酸银溶解度随温度升高而增大 | |
| C. | 60℃时溴酸银的Kap约等于2.5×10-4 | |
| D. | 往溴酸银浊液中滴加NaI有黄色固体生成 |
14.下列反应中,氧化反应与还原反应在同一元素中进行的是( )
| A. | 2FeC12+C12=2FeC13 | B. | Fe+CuSO4=Cu+FeSO4 | ||
| C. | C12+2NaOH=NaC1+NaC1O+H2O | D. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ |