题目内容
【题目】根据下列实验或实验操作和现象,所得结论正确的是
实验或实验操作 | 现象 | 实验结论 | |
A | 用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中 | 出现白色沉淀 | H2CO3的酸性比H2SiO3的酸性强 |
B | 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中含有SO42-、SO32-、HSO3-中的一种或几种 |
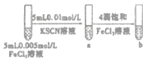
C |
| 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
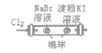
D |
| 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
A. A B. B C. C D. D
【答案】C
【解析】A.盐酸易挥发,盐酸与硅酸钠反应,则不能比较碳酸、硅酸的酸性强弱,A错误;B.先滴加硝酸酸化,再滴加BaCl2溶液,白色沉淀可能为硫酸钡或AgCl,且硝酸具有强氧化性,可氧化亚硫酸根离子,则原溶液中可能存在银离子,B错误;C.增大铁离子浓度,有利于生成络离子,试管b比试管a中溶液的红色深,平衡向正反应方向移动,C正确;D.氯气可氧化溴离子、碘离子,则该实验不能得到Br2>I2,D错误;答案选C。

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案【题目】向盛有不同试剂的试管b中分别滴加适量0.1mol/L FeCl3 溶液,下列对b中现象及解释正确的是
实验 | b中物质 | b中现象 | 结论或解释 | |
| A | Mg(OH)2 悬浊液 | 有红棕色胶体产生 | 发生反应: Fe3++3OH-= Fe(OH)3(胶体) |
B | Cu粉 | 溶液变蓝,试管底部有固体 | 溶液变蓝的原因是: 3Cu+2Fe3+ =2Fe+3Cu2+ | |
C | 5%H2O2溶液 | 有气泡生成 | 该气体为氯气,双氧水有强氧化性氧化Cl- 产生Cl2 | |
D | 饱和NaHCO3溶液 | 有气泡生成,且试管底部有固体 | 发生反应: Fe3++3HCO3-= Fe(OH)3 +3CO2 |
A. A B. B C. C D. D
【题目】表中对于相关物质的分类全部正确的是
编号 | 纯净物 | 混合物 | 碱性氧化物 | 非电解质 |
A | 液氯 | 漂白粉 | Al2O3 | CO |
B | 醋酸 | 浓硫酸 | Na2O2 | 乙醇 |
C | 碱石灰 | 盐酸 | K2O | Cl2 |
D | 胆矾 | 水玻璃 | CaO | SO2 |
A. A B. B C. C D. D