题目内容
14.金刚烷是一种重要的化工原料,工业上可通过下列途径制备: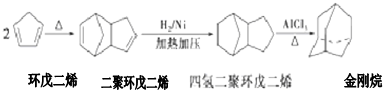
请回答下列问题:
(1)环戊二烯分子中最多有9个原子共平面.
(2)金刚烷的分子式为C10H16.
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
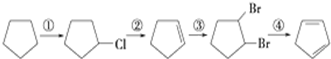
其中,反应②的反应试剂和反应条件是NaOH/醇溶液、加热,反应③的反应类型是加成反应,反应④的化学方程式为
 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr.
+2NaBr.(4)已知烯烃能发生如下反应:
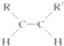 $\stackrel{O_{2}}{→}$ $\stackrel{H_{2}O/Zn}{→}$RCHO+R′CHO.请写出下列反应产物的结构简式:
$\stackrel{O_{2}}{→}$ $\stackrel{H_{2}O/Zn}{→}$RCHO+R′CHO.请写出下列反应产物的结构简式: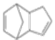 $\stackrel{O_{2}}{→}$ $\stackrel{H_{2}O/Zn}{→}$
$\stackrel{O_{2}}{→}$ $\stackrel{H_{2}O/Zn}{→}$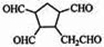 .
.(5)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经酸性高锰酸钾溶液加热氧化可以得到对苯二甲酸(
 ).若考虑苯环上的烯基侧链经酸性高锰酸钾溶液氧化得羧基,写出A所有可能的结构简式(不考虑立体异构):
).若考虑苯环上的烯基侧链经酸性高锰酸钾溶液氧化得羧基,写出A所有可能的结构简式(不考虑立体异构):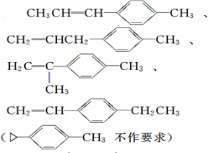 .
.
分析 (1)与双键碳直接相连的原子一定在同一平面内;
(2)根据结构简式判断有机物的分子式和基团数目;
(3)由合成路线可知,反应②为消去反应,反应③为加成反应,反应④为消去反应,以此来解答;
(4)由信息可知,碳碳双键的碳被氧化为醛基;
(5)能使溴的四氯化碳溶液褪色,应含有碳碳双键,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸,说明烃基位于对位位置.
解答 解:(1)C=C为平面结构,与双键碳直接相连的原子一定在同一平面内,则5个C和4个H在同一平面内,
故答案为:9;
(2)由结构简式可知金刚烷的分子式为C10H16,
故答案为:C10H16;
(3)由合成路线可知,反应②为消去反应,反应③为加成反应,反应④为消去反应,
则反应②为卤代烃的消去反应,反应条件为NaOH/醇溶液、加热,反应③类型为加成反应,反应④为 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr,
+2NaBr,
故答案为:NaOH/醇溶液、加热;加成反应; +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr.
+2NaBr.
(4)由信息可知,碳碳双键的碳上含H原子被氧化为醛,则发生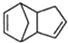 $\stackrel{臭氧}{→}$$\stackrel{水/锌}{→}$
$\stackrel{臭氧}{→}$$\stackrel{水/锌}{→}$ ,
,
故答案为: .
.
(5)能使溴的四氯化碳溶液褪色,应含有碳碳双键,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸,说明烃基位于对位位置,可能的结构有 ,
,
故答案为: .
.
点评 本题考查有机物的合成及结构与性质,注意把握有机物的官能团、碳链骨架等的变化,明确发生的反应及习题中的信息即可解答,题目难度中等.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
4.下列事实不能用平衡移动原理解释的是( )
| A. | 用排饱和食盐水法收集Cl2 | |
| B. | 二氧化硫转化为三氧化硫时增加空气的量以提高二氧化硫的转化率 | |
| C. | 加入催化剂可以提高原料转化率,生成更多产物 | |
| D. | 分别用等体积的蒸馏水和0.01mol/L的硫酸洗涤BaSO4沉淀,用水洗涤造成BaSO4的损失量大于用稀硫酸洗涤的损失量 |
5.某有机物甲经氧化后得到乙(C2H3O2Cl),而甲经水解可得到丙.1mol丙和2mol乙反应可得到一种含氯的酯(C6H8O4Cl2).以此推断甲的结构简式为( )
| A. |  | B. |  | C. |  | D. | HO-CH2-CH2OH |
2.寻找清洁能源一直是化学家努力的方向,下列关于能源的说法错误的是( )
| A. | 氢气热值高,其燃烧产物是水,是一种理想的清洁燃料 | |
| B. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源,保护环境 | |
| C. | 煤的气化技术在一定程度上实现了煤的高效、清洁利用 | |
| D. | 石油作为重要的可再生能源应该被尽量地利用 |
6.某一反应物的浓度是2.0mol/L经4s后变为1.68mol/L,则这4s内平均反应速率为( )
| A. | 0.2mol/(L•S) | B. | 0.1mol/(L•S) | C. | 0.04mol/(L•S) | D. | 0.08mol/(L•S) |
13.如表是部分短周期元素的原子半径及主要化合价.
回答下列问题:
(1)①和⑧能形成原子个数比1:1和2:1的化合物,原子个数比为1:1的化合物中存在的化学键:离子键和非极性共价键.
(2)写出由2个⑦的原子和4个③的原子构成的物质的电子式:
(3)写出④的最高价氧化物对应水化物与①的最高价氧化物对应水化物的水溶液反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(4)下列叙述正确的是ABCD(填字母).
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑧在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
(5)①、⑥、⑧可以形成多种盐,其中一种盐中①、⑥、⑧三种元素的原子个数比为1:1:1,该盐的名称为次氯酸钠.它的水溶液与⑥的氢化物的水溶液反应可生成⑥的单质,该反应的离子方程式为ClO-+2H++Cl-═Cl2↑+H2O.
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(nm) | 0.186 | 0.160 | 0.037 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 |
(1)①和⑧能形成原子个数比1:1和2:1的化合物,原子个数比为1:1的化合物中存在的化学键:离子键和非极性共价键.
(2)写出由2个⑦的原子和4个③的原子构成的物质的电子式:

(3)写出④的最高价氧化物对应水化物与①的最高价氧化物对应水化物的水溶液反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(4)下列叙述正确的是ABCD(填字母).
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑧在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
(5)①、⑥、⑧可以形成多种盐,其中一种盐中①、⑥、⑧三种元素的原子个数比为1:1:1,该盐的名称为次氯酸钠.它的水溶液与⑥的氢化物的水溶液反应可生成⑥的单质,该反应的离子方程式为ClO-+2H++Cl-═Cl2↑+H2O.
 如图为以惰性电极进行电解:
如图为以惰性电极进行电解: ;
; 用中和滴定法测定烧碱的纯度,若烧碱中含有与酸不反应的杂质,试根据实验回答:
用中和滴定法测定烧碱的纯度,若烧碱中含有与酸不反应的杂质,试根据实验回答: