题目内容
4.下列事实不能用平衡移动原理解释的是( )| A. | 用排饱和食盐水法收集Cl2 | |
| B. | 二氧化硫转化为三氧化硫时增加空气的量以提高二氧化硫的转化率 | |
| C. | 加入催化剂可以提高原料转化率,生成更多产物 | |
| D. | 分别用等体积的蒸馏水和0.01mol/L的硫酸洗涤BaSO4沉淀,用水洗涤造成BaSO4的损失量大于用稀硫酸洗涤的损失量 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动,使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答 解:A、氯气和水反应存在Cl2+H2O?HCl+HClO,食盐水中含有氯离子抑制氯气溶解,所以可以采用排饱和食盐水的方法收集氯气,可以用勒夏特里原理解释,故A不选;
B、增大氧气浓度平衡正向移动,可以提高二氧化硫的转化率,所以能用勒沙特列原理解释,能用平衡移动原理解释,故B不选;
C、催化剂只能改变化学反应速率,对化学平衡无影响,不能用平衡移动原理解释,故C选;
D、BaSO4(s)?Ba2++SO42-,用水洗涤使BaSO4的溶解平衡向正方向移动,造成BaSO4的损失;而用H2SO4洗涤,H2SO=2H++SO42-,SO42-的存在抑制了BaSO4的溶解,故BaSO4损失量少,所以能用平衡移动原理解释,故D不选.
故选C.
点评 本题考查平衡移动原理知识,题目难度不大,注意使用平衡移动原理的前提必须是可逆反应,平衡发生移动.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下列微粒中半径最小的( )
| A. | Na+ | B. | Al3+ | C. | K+ | D. | S2- |
15.关于电解法精炼铜的下列说法正确的是( )
| A. | 电解结束后,在阳极底部会有阳极泥产生,主要成分是铁、金和银 | |
| B. | 电解结束后,溶液中Cu2+浓度变大 | |
| C. | 纯铜作阳极,粗铜作阴极,硫酸铜为电解质溶液 | |
| D. | 粗铜作阳极,纯铜作阴极,硫酸铜为电解质溶液 |
12.下列有关实验叙述错误的是( )
| A. | 实验室可用硫酸铜溶液除去乙炔中的H2S等杂质气体 | |
| B. | 苯和溴水在溴化铁溶液催化作用下发生取代反应生成溴苯 | |
| C. | 只用溴水就可以将苯、四氯化碳、酒精、氢氧化钠溶液这四种物质区别开 | |
| D. | 将铜丝在酒精灯上加热变黑后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
19.生活中处处有化学,下列表述不正确的是( )
| A. | 福尔马林可作食品的保鲜剂 | |
| B. | 苯酚有毒,但可用于杀菌消毒 | |
| C. | 聚乙烯塑料制品可用于食品的包装 | |
| D. | 食醋的主要成分是醋酸,它是一种弱酸 |
9.1,3-丁二烯和2-丁炔分别与氢气反应的热化学方程式如下:
CH2=CH-CH=CH2(g)+2H2(g)=CH3CH2CH2CH3(g)△H=-236.6kJ•mol-1
CH3-C≡C-CH3(g)+2H2(g)=CH3CH2CH2CH3(g)△H=-272.7kJ•mol-1
由此不能判断( )
CH2=CH-CH=CH2(g)+2H2(g)=CH3CH2CH2CH3(g)△H=-236.6kJ•mol-1
CH3-C≡C-CH3(g)+2H2(g)=CH3CH2CH2CH3(g)△H=-272.7kJ•mol-1
由此不能判断( )
| A. | 1,3-丁二烯和2-丁炔稳定性的相对大小 | |
| B. | 1,3-丁二烯和2-丁炔分子储存能量的相对高低 | |
| C. | 1,3-丁二烯和2-丁炔相互转化的热效应 | |
| D. | 一个碳碳叁键的键能与两个碳碳双键键能之和的大小 |
16.230Th和232Th是钍的两种同位素,232Th可以转化成233U.下列有关Th的说法正确的是( )
| A. | Th元素的质量数是232 | B. | 230Th和232Th的化学性质相同 | ||
| C. | 232Th转化成233U是化学变化 | D. | Th元素的相对原子质量是231 |
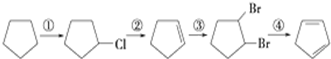
 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr.
+2NaBr.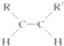 $\stackrel{O_{2}}{→}$ $\stackrel{H_{2}O/Zn}{→}$RCHO+R′CHO.请写出下列反应产物的结构简式:
$\stackrel{O_{2}}{→}$ $\stackrel{H_{2}O/Zn}{→}$RCHO+R′CHO.请写出下列反应产物的结构简式: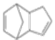 $\stackrel{O_{2}}{→}$ $\stackrel{H_{2}O/Zn}{→}$
$\stackrel{O_{2}}{→}$ $\stackrel{H_{2}O/Zn}{→}$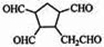 .
. ).若考虑苯环上的烯基侧链经酸性高锰酸钾溶液氧化得羧基,写出A所有可能的结构简式(不考虑立体异构):
).若考虑苯环上的烯基侧链经酸性高锰酸钾溶液氧化得羧基,写出A所有可能的结构简式(不考虑立体异构):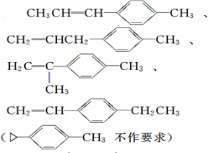 .
.