题目内容
15.下列说法中,正确的是( )| A. | 任何溶液中,c(H+)×c(OH-)=1.0×10-14 | |
| B. | pH=0的溶液呈中性 | |
| C. | 酸性溶液中,c(H+)越大,酸性越强 | |
| D. | 酸性溶液中没有OH-,碱性溶液里没有H+ |
分析 A.水的离子积常数与温度有关,与溶液酸碱性无关;
B.pH=0的溶液可能呈酸性;
C.酸性溶液中,c(H+)与溶液酸性成正比;
D.任何水作溶剂的电解质溶液中都含有氢离子、氢氧根离子.
解答 解:A.水的离子积常数与温度有关,与溶液酸碱性无关,温度不同c(H+)×c(OH-)不一定等于1.0×10-14,故A错误;
B.常温下,pH=0的溶液呈酸性,故B错误;
C.酸性溶液中,c(H+)与溶液酸性成正比,所以c(H+)越大,酸性越强,故C正确;
D.任何水作溶剂的电解质溶液中都含有氢离子、氢氧根离子,所以酸性溶液中含有氢离子、氢氧根离子,只是存在c(H+)>c(OH-),故D错误;
故选C.
点评 本题考查探究溶液酸碱性,溶液酸碱性要根据溶液中c(H+)、c(OH-)相对大小判断,温度未知时不能根据溶液pH判断,易错选项是A.

练习册系列答案
相关题目
4.进行一氯取代反应后,只能生成3种沸点不同的有机产物的烷烃是( )
| A. | (CH3)2CHCH2CH2CH3 | B. | (CH3)3CCH2CH3 | C. | (CH3)2CHCH(CH3)2 | D. | (CH3CH2)2CHCH3 |
6.下列各项叙述正确的是( )
| A. | 从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增的 | |
| B. | Na在氧气中燃烧主要生成Na2O | |
| C. | 第3周期非金属元素含氧酸的酸性从左到右依次增强 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
3.下列检验离子的方法及现象描述正确的是( )
| A. | 检验SO42-:加入BaCl2溶液出现白色沉淀,再加足量稀HCl沉淀不溶解 | |
| B. | 检验Cl-:确定无SO42-后,加入AgNO3溶液出现白色沉淀,加入足量稀HNO3沉淀不溶解 | |
| C. | 检验Na+:将干净的铂丝蘸取少量溶液在酒精灯上灼烧,观察火焰呈黄色 | |
| D. | 检验NH4+:滴入NaOH溶液后,加热,用湿润蓝色石蕊试纸检验发现变红 |
20.向如图所示的装置中缓慢地通入气体X,若关闭活塞K,则品红溶液无变化而澄清石灰水变浑浊;若打开活塞K,则品红溶液褪色.X和Y可能是( )
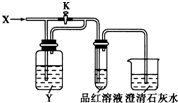
| A | B | C | D | |
| X | SO2 | Cl2 | HCl | NO2 |
| Y | NaHCO3 溶液 | 饱和Na2SO3溶液 | 饱和NaCl溶液 | 水 |

| A. | A | B. | B | C. | C | D. | D |
7.某主族元素的电离能(单位:kJ•mol-1)如下表,此元素位于元素周期表的族数是( )
| I1 | I2 | I3 | I4 | I5 | I6 | I7 |
| 1011.8 | 1907 | 2914.1 | 4963.6 | 6273.9 | 21267 | 25431 |
| A. | ⅢA | B. | ⅣA | C. | ⅤA | D. | ⅥA |
4.如图是某有机物的质谱图,其相对分子质量为( )
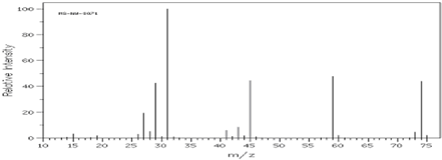

| A. | 74 | B. | 31 | C. | 59 | D. | 45 |
5.按所示格式填写下表:
| 原子序数 | 电子排布式 | 价层电子排布 | 周期 | 族 |
| 8 | 1s22s22p4 | 2s22p4 | 第二周期 | ⅥA |
| 24 | 1s22s22p63s23p63d54s1 | 3d54s1 | 第四周期 | ⅥB |
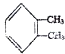 ;若C8H10分子中苯环上的一氯代物有三种,则其结构简式为
;若C8H10分子中苯环上的一氯代物有三种,则其结构简式为 或
或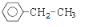 .
.