题目内容
8.利用如图所示装置进行下列实验,能得出相应实验结论的是( )| 选项 | ① | ② | ③ | 实验结论 | 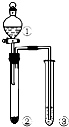 |
| A | NaCl溶液 | 电石 | 酸性KMnO4 | 乙炔具有还原性 | |
| B | 浓硝酸 | Na2CO3 | 苯酚钠溶液 | 酸性:硝酸>碳酸>苯酚 | |
| C | 浓盐酸 | KMnO4 | FeBr2(足量) | 氧化性:Cl2>Br2 | |
| D | 浓硫酸 | 蔗糖 | 溴水 | 浓硝酸具有脱水性、氧化性 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.乙炔中混有硫化氢等气体;
B.浓硝酸与碳酸钠反应生成二氧化碳,但浓硝酸易挥发,硝酸、碳酸均可与苯酚钠溶液反应生成.
C.氯气先氧化亚铁离子;
D.浓硫酸使蔗糖变黑,然后C与浓硫酸发生氧化还原反应生成二氧化硫,二氧化硫与溴水发生氧化还原反应使其褪色.
解答 解:A.乙炔中混有硫化氢等气体,可与酸性高锰酸钾发生氧化还原反应,应先除杂,故A错误;
B.浓硝酸与碳酸钠反应生成二氧化碳,但浓硝酸易挥发,硝酸、碳酸均可与苯酚钠溶液反应生成,应先除杂,否则不能证明碳酸>苯酚,故B错误;
C.亚铁离子还原性大于溴离子,如氯气不足,则不能生成溴,不能排出亚铁离子的影响,故C错误;
D.浓硫酸具有脱水性使蔗糖变黑,然后C与浓硫酸发生氧化还原反应生成二氧化硫,体现其强氧化性,最后二氧化硫与溴水发生氧化还原反应使其褪色,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及氯气的制备、浓硫酸的性质、酸性比较、氧化还原反应等,把握化学反应原理及实验装置中的反应为解答的关键,注意实验操作的可行性、评价性分析,题目难度不大.

练习册系列答案
相关题目
16.下列叙述正确的是( )
| A. | 室温下a L稀氨水与b L稀硫酸反应后,溶液pH=7时,c(SO42- )>c(NH4+) | |
| B. | 室温下pH=11的氨水与pH=3的盐酸等体积混合,滴人酚酞溶液呈红色 | |
| C. | 室温下两种醋酸溶液的物质的量浓度分别为c1和c2,pH依次分别为a和a+1,则Cl=l0C2 | |
| D. | 将10 mL 0.1 mol/L Na2CO3溶液逐滴滴加到10mL 0.1 mol/L盐酸中,所得溶液 c(Na+)>c(Cl-)>c(HCO3- )>c(CO32-) |
13.化学是一门实用性强的自然科学,在社会、生产、生活中起着重要的作用,下列说法正确的是( )
| A. | 金属钾具有强还原性,可用其余TiCl溶液反应制取金属Ti | |
| B. | 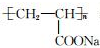 表示一种易溶于水的高分子树脂 表示一种易溶于水的高分子树脂 | |
| C. | 由于Si是一种很重要的半导体材料,故常用其来制作信息的传到材料-光导纤维 | |
| D. | 山东东营广饶县一男子子收到网购物品后,因吸人氟乙酸甲酯中毒身亡,氟乙酸甲酯的结构简式为FCH2COOCH3能与H2发生加成反应.也能被LiAlH4还原 |
20.短周期元素X、Y、Z在元素周期表中的位置如图,已知X与Y的原子序数之和等于Z的原子序数.下列说法错误的是( )
| X | Y | |
| Z |
| A. | Y的气态氢化物比X的最简单气态氢化物的稳定性高 | |
| B. | 在X、Y、Z三种元素中,只有X的最高价氧化物对应的水化物与它的气态氢化物可以反应生成盐 | |
| C. | 由X、Y、Z分别形成的单质,常温下Z单质的沸点最高 | |
| D. | 在标准状况下,1molY 的氢化物的体积约为22.4L |
17.分类是重要的科学研究方法,下列物质分类错误的是( )
| A. | 电解质:明矾、碳酸、硫酸钡 | B. | 酸性氧化物:SO3、CO2、NO | ||
| C. | 混合物:铝热剂、矿泉水、焦炉气 | D. | 同素异形体:C60、C70、金刚石 |
18.某新研制药品的主要成分结构如下所示.关于其说法不正确的是( )


| A. | 其分子为C8H8O2•H2O | |
| B. | 该物质属于水合物 | |
| C. | 1 mol该物质可与3 mol H2发生加成反应 | |
| D. | 该有机物属于芳香烃类 |
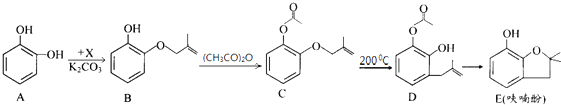
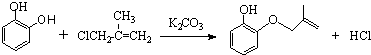 .
. .
. 磷单质及其化合物有广泛应用.
磷单质及其化合物有广泛应用. )之间脱去两个水分子的产物,其结构简式为
)之间脱去两个水分子的产物,其结构简式为 .三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
.三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.