题目内容
13.化学是一门实用性强的自然科学,在社会、生产、生活中起着重要的作用,下列说法正确的是( )| A. | 金属钾具有强还原性,可用其余TiCl溶液反应制取金属Ti | |
| B. | 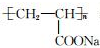 表示一种易溶于水的高分子树脂 表示一种易溶于水的高分子树脂 | |
| C. | 由于Si是一种很重要的半导体材料,故常用其来制作信息的传到材料-光导纤维 | |
| D. | 山东东营广饶县一男子子收到网购物品后,因吸人氟乙酸甲酯中毒身亡,氟乙酸甲酯的结构简式为FCH2COOCH3能与H2发生加成反应.也能被LiAlH4还原 |
分析 A.钾性质强于钠,与盐溶液反应先与水反应;
B高吸水性树脂是具有许多亲水基团的低交联度或部分结晶的高分子聚合物;
C.光导纤维主要成分为二氧化硅;
D.氟乙酸甲酯的结构简式为FCH2COOCH3,属于酯类不能和氢气加成,不能被LiAlH4还原.
解答 解:A.钾放入TiCl溶液中先与溶液中的水反应,不会置换金属Ti,故A错误;
B.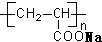 具有许多亲水基团的低交联度,是一种吸水性高分子树脂,故B正确;
具有许多亲水基团的低交联度,是一种吸水性高分子树脂,故B正确;
C.光导纤维主要成分为二氧化硅,不是硅,故C错误;
D.氟乙酸甲酯的结构简式为FCH2COOCH3,属于酯类不能和氢气加成,不能被LiAlH4还原,故D错误;
故选:B.
点评 本题考查了元素化合物知识,熟悉钠、材料组成、有机物性质是解题关键,题目难度不大.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目
4.设NA为阿伏伽德罗常数的值,下列说法中正确的是( )
| A. | 标准状况下11.2L乙烯和丙烯的混合气体中含C-H键的数目为2NA | |
| B. | S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA | |
| C. | 0.5mol熔融的NaHSO4中含有的离子数目为1.5NA | |
| D. | 含0.2molH2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA |
1.设NA代表阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 25℃时,pH=11的Na2CO3溶液中水电离出来的H+数目为10-3NA | |
| B. | 78gNa2S和Na2O2的混合物中阴离子的数目为2NA | |
| C. | 在标准状况下,11.2LCCI4分子中氯原子数目为2NA | |
| D. | 室温下,4.4g乙醛和乙酸乙酯的混合物中含有碳原子数目为0.2NA |
8.利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 | 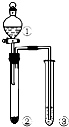 |
| A | NaCl溶液 | 电石 | 酸性KMnO4 | 乙炔具有还原性 | |
| B | 浓硝酸 | Na2CO3 | 苯酚钠溶液 | 酸性:硝酸>碳酸>苯酚 | |
| C | 浓盐酸 | KMnO4 | FeBr2(足量) | 氧化性:Cl2>Br2 | |
| D | 浓硫酸 | 蔗糖 | 溴水 | 浓硝酸具有脱水性、氧化性 |
| A. | A | B. | B | C. | C | D. | D |
18.下列有关实验操作的解释或纵论正确的是( )
| 选项 | 实验操作 | 解释或结论 |
| A | 向某溶液中滴加盐酸酸化的BaCl2溶液,出现白色沉淀 | 溶液中一定含有SO42- |
| B | 将某气体通入品红溶液中溶液褪色,加热褪色后的溶液,溶液又恢复原色 | 该气体为SO2 |
| C | 用蒸馏水润湿的pH试纸测溶液的pH | 一定会使测定结果偏低 |
| D | 向混有乙酸和乙醇的乙酸乙酯中加入氢氧化钠溶液 | 除溶液中的乙酸和乙醇 |
| A. | A | B. | B | C. | C | D. | D |
5.聚乳酸是一种生物降解塑料,结构简式为  .下列说法正确的是( )
.下列说法正确的是( )
 .下列说法正确的是( )
.下列说法正确的是( )| A. | 聚乳酸的相对分子质量是72 | B. | 聚乳酸的分子式是C3H4O2 | ||
| C. | 乳酸的分子式是C3H6O2 | D. | 聚乳酸可以通过水解降解 |
2.如图是部分短周期元素原子半径与原子序数的关系图.字母代表元素,分析正确的是( )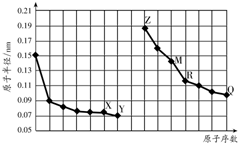

| A. | R在周期表的第15列 | |
| B. | Y、Q两种元素的气态氢化物及其最高价氧化物的水化物均为强酸 | |
| C. | 简单离子的半径:X>Z>M | |
| D. | Z的单质能从M与Q元素构成的盐溶液中置换出单质M |
3.向4.0L容器中充入0.70 mol SO2和0.40 mol O2,4s后测得剩余SO2 0.30 mol,则v(O2)为( )
| A. | 0.10 mol•L-1•s-1 | B. | 0.025 mol•L-1•s-1 | ||
| C. | 0.50 mol•L-1•s-1 | D. | 0.0125 mol•L-1•s-1 |
