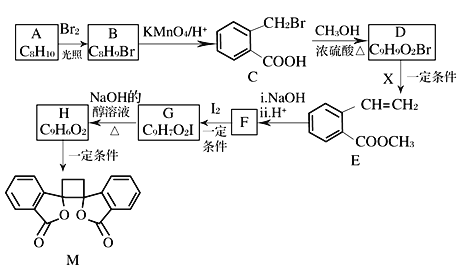
题目内容
【题目】下列离子方程式中,不正确的是
A. 二氧化锰与浓盐酸加热反应:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
B. 氯化镁溶液与氨水反应:Mg2++2NH3·H2O=Mg(OH)2↓+2NH
C. 金属钠与水反应:2Na+2H2O=2Na++2OH-+H2↑
D. 氯化铁溶液与碘化钾溶液反应:Fe3++2I-=Fe2++I2
【答案】D
【解析】
A.二氧化锰与浓盐酸加热反应生成氯气、氯化锰和水,该反应的离子方程式为:MnO2+4H++2Cl- ![]() Mn2++Cl2↑+2H2O,故A正确;B.氨水为弱碱,氯化镁溶液与氨水反应的离子方程式为:Mg2++2NH3H2O=Mg(OH)2↓+2NH4+,故B正确;C.金属钠与水反应生成NaOH和氢气,反应的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故C正确;D.氯化铁溶液与碘化钾溶液反应生成氯化亚铁和碘单质,方程式的电荷不守恒,正确的离子方程式为:2Fe3++2I-=2Fe2++I2,故D错误;故选D。
Mn2++Cl2↑+2H2O,故A正确;B.氨水为弱碱,氯化镁溶液与氨水反应的离子方程式为:Mg2++2NH3H2O=Mg(OH)2↓+2NH4+,故B正确;C.金属钠与水反应生成NaOH和氢气,反应的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,故C正确;D.氯化铁溶液与碘化钾溶液反应生成氯化亚铁和碘单质,方程式的电荷不守恒,正确的离子方程式为:2Fe3++2I-=2Fe2++I2,故D错误;故选D。

【题目】硫代硫酸钠(Na2S2O3·5H2O) 俗名“大苏打”。易溶于水,难溶于乙醇,沸点为100℃,酸性或加热条件下易分解。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:
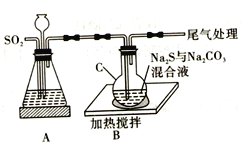
回答下列问题:
(1)装置A可用于观察SO2的生成速率,其中的液体最好选择_____________(填序号)。若装置堵塞使气流不畅,则A中的现象为_______________________________。
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(2)尾气处理可以选择以下装置中的________(填序号)。
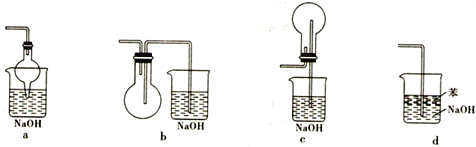
(3)反应过程中若pH值小于7则会降低产率,请用离子方程式解释原因:_________________________。
(4)请写出装置C中发生反应的化学方程式:_________________________。
(5)反应结束后,取C中混合物趁热过滤,取滤液于蒸发皿中, ______________,抽滤,洗涤,低温下干燥得产品。洗涤时要尽量减少产品的损失,其具体操作是_________________________。
(6)为检验制得的产品的纯度,该实验小组称取4g 的产品配制成250mL 硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入20mL 0.0lmol·L-1KIO3溶液,并加入过量的KI并酸化,发生下列反应:5I-+IO3-+6H+=3I2+3H2O,再加入几滴淀粉溶液,立即用所配的Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+ S4O62-,实验数据如下表:
实验序号 | 1 | 2 | 3 |
Na2S2O3溶液体积(mL) | 19.98 | 20.02 | 21.2 |
当滴入最后一滴Na2S2O3溶液时,溶液___________,且半分钟内不变化,则达到终点。计算该产品的纯度是____________________________。