题目内容
【题目】在一定温度下,氯气与NaOH溶液反应可生成NaCl、NaClO和NaClO3。下列判断不正确的是( )
A.若反应过程中消耗2mol氯气,则转移电子数目可能为3NA
B.反应停止后n(NaClO):n(NaCl):n(NaClO3)可能为1:6:1
C.氯气与氢氧化钠反应过程中消耗氯气与NaOH的物质的量之比一定为1:2
D.若氢氧化钠与氯气恰好完全反应,则反应后所得溶液中总是存在:c(Na+)=c(Cl-)+c(ClO-)+c(ClO3-)
【答案】D
【解析】
A.若氯气与NaOH发生3Cl2+6NaOH=5NaCl+NaClO3+3H2O转移电子数最多,1mol转移![]() mol电子;发生Cl2+2NaOH=NaCl+NaClO+H2O转移电子最少,转移1mol电子,2mol氯气反应,可能转移3mol电子,A判断正确;
mol电子;发生Cl2+2NaOH=NaCl+NaClO+H2O转移电子最少,转移1mol电子,2mol氯气反应,可能转移3mol电子,A判断正确;
B.反应停止时,n(NaClO):n(NaCl):n(NaClO3)为1:6:1时,得电子数目为1×1+5×1=6,失电子数目为1×6,相等,B判断正确;
C.根据NaCl、NaClO、NaClO3可知,钠离子和氯原子的物质的量之比为1:1,则参加反应所需氯气与NaOH的物质的量之比为1:2,C判断正确;
D.根据溶液中离子电荷守恒,c(Na+)+c(H+)=c(Cl-)+c(ClO-)+c(OH-)+3c(ClO3-),D判断错误;
答案为D。

【题目】某实验小组用软锰矿制备高锰酸钾,主要实验步骤如下:
步骤一:将软锰矿(主要成分为MnO2)、KClO3和KOH固体按一定比例混合后加热熔融可制得绿色K2MnO4;
步骤二:将反应后固体充分溶解、过滤,向滤液中通入过量CO2气体使溶液显酸性,K2MnO4在酸性条件下反应得到KMnO4、MnO2和K2CO3,最后分离得到高锰酸钾晶体(粗产品)。
请回答下列问题:
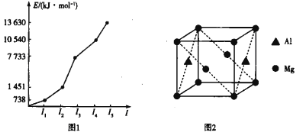
(1)步骤一加热熔融应在________(填序号)进行。
A.铁坩埚 B.氧化铝坩埚 C.瓷坩埚 D.石英
(2)为进一步提高粗产品(高锰酸钾晶体)的纯度,常采用的实验方法是_____________。
(3)KMnO4、MnO2在一定条件下都可以氧化浓盐酸制取氯气,制取等物质的量的氯气消耗KMnO4与MnO2的物质的量之比为________________。
(4)某学习小组为了探究高锰酸钾溶液和草酸钠溶液的反应过程,将高锰酸钾溶液逐滴滴入一定体积的酸性草酸钠溶液中(温度相同,并不断振荡),记录的现象如表:
滴入KMnO4溶液的次序(假设每滴溶液体积相等) | 滴入的KMnO4溶液紫色褪去的时间 |
先滴入第1滴 | 1min |
褪色后再滴入第2滴 | 15s |
褪色后再滴入第3滴 | 3s |
褪色后再滴入第4滴 | 1s |
请分析高锰酸钾溶液褪色时间变化的原因:_________。
(5)我国《室内空气质量标准》规定室内空气中甲醛(HCHO)含量不得超过0.08mg/m3。我校某同学通过查阅资料,拟采用如下方法测定2019年暑假新装修的焕然一新的明德楼教室内空气中甲醛的含量。
测定原理:5HCHO+4KMnO4+6H2SO4=2K2SO4+4MnSO4+5CO2↑+11H2O。
实验操作:用容积为1000mL用注射器抽取空气,缓慢注入酸性高锰酸钾溶液中(装置如图),当酸性高锰酸钾溶液正好褪色时,停止注入。

①用0.1000mol/L的酸性KMnO4溶液配制实验中使用的酸性KMnO4溶液l000mL,需0.1000mol/L的酸性KMnO4溶液的体积为___________。
②装置中多孔玻璃球泡的作用是__________。
③该同学在206教室内不同地点抽取空气,并缓慢注入酸性高锰酸钾溶液中。当第250次将注射器中空气全部缓慢注入酸性高锰酸钾溶液中时,酸性高锰酸钾溶液恰好褪色。请通过计算判断,该教室空气中甲醛含量________(填“已”或“未”)超标。若未超标,该教室内空气中甲醛(HCHO)含量为________mg/m3;若已超标,请举出减少室内空气污染的一条合理措施:_________________。