题目内容
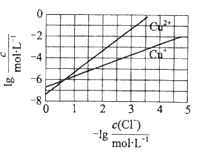
【题目】在湿法炼锌的电解循环溶液中,较高浓度的Cl会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是
A. Ksp(CuCl)的数量级为![]()
B. 除Cl反应为Cu+Cu2++2Cl![]() 2CuCl
2CuCl
C. 加入Cu越多,Cu+浓度越高,除Cl效果越好
D. 2Cu+![]() Cu2++Cu平衡常数很大,反应趋于完全
Cu2++Cu平衡常数很大,反应趋于完全
【答案】C
【解析】A.由图像可知,横坐标为1时,lgc(Cu+)大于-6,则Ksp(CuCl)的数量级为10-7,故A正确;B.涉及反应物为铜、硫酸铜以及氯离子,生成物为CuCl,反应的方程式为Cu+Cu2++2Cl-=2CuCl,故B正确;C.根据反应Cu+Cu2++2Cl-=2CuCl,反应的效果取决于Cu2+的浓度,如Cu2+不足,则加入再多的Cu也不能改变效果,故C错误;D.酸性条件下,Cu+不稳定,易发生2Cu+=Cu2++Cu,可知没有Cl-存在的情况下,2Cu+=Cu2++Cu趋向于完全,说明2Cu+=Cu2++Cu的平衡常数很大,故D正确;故选C。

【题目】25℃时,浓度均为0.1 mol/L的溶液,其pH如下表所示。有关说法正确的是
序号 | ① | ② | ③ | ④ |
溶液 | NaCl | CH3COONH4 | NaF | NaHCO3 |
pH | 7.0 | 7.0 | 8.1 | 8.4 |
A.酸性强弱:H2CO3>HF
B.①和②中溶质均未水解
C.离子的总浓度:①>③
D.④中:c(HCO3-) + 2c(CO32-) + c(H2CO3)![]() 0.1 mol/L
0.1 mol/L
【题目】N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g) ![]() 4NO2(g)+O2(g) ΔH>0,T1温度下的部分实验数据为:
4NO2(g)+O2(g) ΔH>0,T1温度下的部分实验数据为:
t/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/(mol·L-1) | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是( )
A. 500 s内N2O5分解速率为2.96×10-3 mol·L-1·s-1
B. 其他条件不变,T2温度下反应到1000s时测得N2O5(g)浓度为2.98 mol·L-1,则T1<T2
C. T1温度下的平衡常数为K1=125,1000s时转化率为50%
D. T1温度下的平衡常数为K1,T3温度下的平衡常数为K3,若K1>K3,则T1>T3