题目内容
5.某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标准状况下,将44.8L混合气体通入足量溴水,溴水质量增重28.0g,通过计算回答:(1)混合气体中气态烷烃的分子式:CH4.
(2)混合气体中烷烃与烯烃的物质的量之比:n(CH4):n(烯烃)=3:1.
(3)写出混合气体中气态烯烃可能的结构简式(不考虑顺反异构):CH2=CH-CH2CH3、CH3-CH=CH-CH3、CH2=C(CH3)2.
分析 (1)相同条件下,密度之比等于相对分子质量之比,据此计算混合气体的相对分子质量,进而确定含有的烷烃;
(2)根据n=$\frac{V}{{V}_{m}}$计算44.8L混合气体的物质的量,再根据m=nM计算混合气体的质量,溴水质量增重28g为烯烃的质量,进而计算烷烃的质量与物质的量,再计算烯烃的物质的量,据此解答;
(3)由烯烃的质量与物质的量,根据M=$\frac{m}{n}$计算其摩尔质量,据此计算烯烃的分子式,书写可能的结构.
解答 解:(1)在同温同压下,混合气体对氢气的相对密度为13,故混合气体的平均相对分子质量为:13×2=26,烯烃中相对分子质量最小的为乙烯的28,故一定含有甲烷,
故答案为:CH4;
(2)标况下44.8L混合气体的物质的量为:$\frac{44.8L}{22.4L/mol}$=2mol,故混合气体的总质量为:2mol×26g/mol=52g,溴水质量增重28g为烯烃的质量,故甲烷的质量为:52g-28g=24g,故甲烷的物质的量为:$\frac{24g}{16g/mol}$=1.5mol,
烯烃的物质的量为:2mol-1.5mol=0.5mol,故n(CH4):n(烯烃)=1.5mol:0.5mol=3:1,
故答案为:n(CH4):n(烯烃)=3:1;
(3)烯烃的摩尔质量为$\frac{28g}{0.5mol}$=56g/mol,设烯烃的组成为(CH2)n,故14n=56,解得n=4,故该烯烃为C4H8,可能的结构为:CH2=CH-CH2CH3,CH3-CH=CH-CH3,CH2=C(CH3)2,
故答案为:CH2=CH-CH2CH3、CH3-CH=CH-CH3、CH2=C(CH3)2.
点评 本题以计算题形式考查有机物的推断、同分异构体等知识,题目难度中等,根据平均相对分子质量确定含有甲烷是解题的关键,注意掌握常见有机物结构与性质的关系.

 阅读快车系列答案
阅读快车系列答案| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
| A. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 | |
| B. | 相同浓度和体积的强酸与强碱溶液混合后,溶液的PH=7 | |
| C. | 向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 | |
| D. | 若反应2A(g)+B(g)=2C(g)在一定条件下是一个自发的反应,则该反应为吸热反应 |
| A. | 氢氧化铝和硝酸溶液反应 | B. | Fe(OH)3溶液和硫酸反应 | ||
| C. | 氢氧化钡溶液和稀硫酸 | D. | KOH溶液和稀硝酸反应 |
| A. | A沸点比B高 | |
| B. | A相对密度比B小 | |
| C. | 一般情况下,同碳原子的烷烃的沸点和密度低于烯烃 | |
| D. | 已知A在常温下为液态,则B不可能为气态 |
| A. | 硅原子和钠原子 | B. | 硼原子和氦原子 | C. | 氯原子和碳原子 | D. | 碳原子和铝原子 |
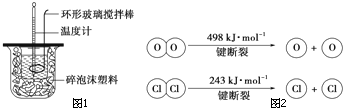 针对化学反应中的能量变化解决下列问题.
针对化学反应中的能量变化解决下列问题.