题目内容
【题目】请回答下列问题。
(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度。
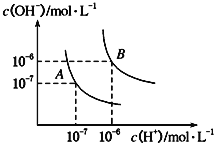
①100℃时1mol·L-1的NaOH溶液中,由水电离出的c(H+)=______mol·L-1,Kw(25℃)________Kw(100℃) (填“>”、“<”或“=”)。
②25℃时,向水的电离平衡体系中加入少量 NH4Cl固体,对水的电离平衡的影响是_____(填“促进”、“抑制”或“不影响”)。
(2)电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
化学式 | 电离平衡常数(25℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25℃时,有等浓度的a.NaCN溶液 b.CH3COONa 溶液 c.Na2CO3溶液,三种溶液的pH由大到小的顺序为_____________________;(填序号)
②25℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,则c(Na+) c(CH3COO-) (填“>”、“<”或“=”);
【答案】(1)① 1×10-12 < ② 促进;(2)①c>a>b ② >;
【解析】试题分析:(1)25℃时纯水中c(H+)=c(OH-)=10-7mol/L,Kw=c(H+)c(OH-)=10-14 ,当温度升高到100℃,纯水中c(H+)=c(OH-)=10-6mol/L,Kw=c(H+)c(OH-)=10-12 ;
100℃时1molL-1的NaOH溶液中Kw=c(H+)c(OH-)=10-12 ;c(OH-)=1mol/L,水电离出的c(H+)=1×10-12;水电电离是吸热反应,温度升高,水的电离程度增大,Kw增大,因此Kw(25℃)<Kw(100℃) 。NH4Cl固体溶解后溶液中铵根离子水解生成一水合氨和氢离子,溶液呈酸性,水的电离被促进;故答案为:1×10-12;<;促进;
(2)①依据图表数据分析,醋酸电离常数大于氰酸大于碳酸氢根离子,所以等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液水解程度等浓度的Na2CO3溶液>NaCN溶液>CH3COONa溶液,溶液pH为Na2CO3溶液的>NaCN溶液的>CH3COONa溶液的;故答案为:Na2CO3溶液>NaCN溶液>CH3COONa溶液;
②等浓度的CH3COOH溶液和NaOH溶液等体积混合,所得溶液显碱性,c(H+)<c(OH-)依据溶液中电荷守恒c(H+)+c(Na+)=c(OH-)+c(CH3COO-),c(Na+)>c(CH3COO-);故答案为:>。

 智能训练练测考系列答案
智能训练练测考系列答案【题目】用中和滴定法测定烧碱的纯度,若烧碱中不含有与酸反应的杂质,试根据实验回答:
(1)准确称取4.1g烧碱样品。
(2)将样品配成250mL待测液,需要的仪器除了小烧杯、玻璃棒、量筒还需要____________________。
(3)取10.00mL待测液,用___________________ 量取。
(4)用0.2010mol·L-1标准盐酸滴定待测烧碱溶液,甲基橙做指示剂,滴定时左手旋转滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视____________,至出现______________的现象时即到达滴定终点。
(5)根据下列数据,计算待测烧碱的纯度:__________________。(保留四位有效数字)
滴定次数 | 待测液体积 (mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 10.00 | 0.50 | 20.40 |
第二次 | 10.00 | 0.10 | 22.10 |
第三次 | 10.00 | 4.00 | 24.10 |
(6)以下操作会造成测量结果偏高的是(_________)
①用蒸馏水冲洗锥形瓶;
②在滴定过程中不慎将数滴酸液滴在锥形瓶外;
③读数时,滴定前仰视,滴定后俯视;
④装标准液之前,没有用标准液润洗滴定管;
【题目】X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示:
X | Y | Z | M | R | Q | |
原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
主要化合价 | -4,+4 | -2 | -1, +7 | +3 | ||
其他 | 阳离子核 外无电子 | 无机非金属 材料的主角 | 焰色反 应呈黄色 |
(1) R在元素周期表中的位置是____;R在自然界中有质量数为35和37的两种核素,它们之间的关系互为 __________________________________________
(2) 根据表中数据推测,Y的原子半径(用r表示)的最小范围是____________。
(3)Y与R相比,非金属性较强的是____(用元素符号表示),下列事实能证明这一结论的是___(选填字母序号)。
A.常温下Y的单质呈固态,R的单质呈气态
B.稳定性XR>YX4
C.Y最高价氧化物对应水化物的酸性弱于R最高价氧化物对应水化物的酸性
(4)用电子式表示X2M___________。
(5) Z的单质与水反应的化学方程式是____________________________。