题目内容
下列说法可以证明反应:N2+3H2
2NH3已达平衡状态的是( )
| 催化剂 |
| 高温、高压 |
| A、一个N≡N键断裂的同时,有3个H-H键形成 |
| B、N2、H3、NH3的分子数之比为1:3:2 |
| C、一个N≡N键断裂的同时,有6个N-H键形成 |
| D、N2、H2、NH3的浓度不再变化 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、1个 N≡N键断裂的同时,有3个 H-H键生成,正逆反应速率相等,达到了平衡状态,故A正确;
B、平衡时各物质的物质的量浓度之比取决于物质的起始浓度和转化率,故各物质的物质的量浓度之比不能作为判断是否达到平衡状态的依据,故B错误;
C、一个N≡N键断裂的同时,有6个N-H键形成,都表示正速率,不能判断反应是否达到平衡状态,故C错误;
D、当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,所以N2、H2、NH3的浓度不再变化,说明反应达到了平衡状态,故D正确;
故选AD.
B、平衡时各物质的物质的量浓度之比取决于物质的起始浓度和转化率,故各物质的物质的量浓度之比不能作为判断是否达到平衡状态的依据,故B错误;
C、一个N≡N键断裂的同时,有6个N-H键形成,都表示正速率,不能判断反应是否达到平衡状态,故C错误;
D、当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,所以N2、H2、NH3的浓度不再变化,说明反应达到了平衡状态,故D正确;
故选AD.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为零,属于基础知识的考查.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
NA为阿伏加德罗常数,下列叙述错误的是( )
| A、26g C2H2和苯蒸气的混合气体中所含的C原子数为2NA |
| B、12g金刚石中含有的共价键键数为4NA |
| C、0.1mol NaHCO3晶体中含0.2NA个离子 |
| D、1mol甲基(-CH3)所含电子数为9NA |
下列叙述与对应图式正确的是( )
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 主要化合价 | -2 | +2 | +1 | +5、-3 | +7、-1 | +1 | +5、-3 | +3 |
| A、由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强 |
B、 如图装置中,待镀铁制品应与电源负极相连 |
C、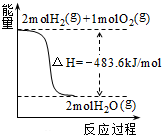 如图表示H2与O2发生反应过程中的能量变化,则H2的燃烧热的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol |
D、 如图表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变 |
某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→O2.则下列说法中正确的是( )
| A、上述过程的氧化剂为H2O2 | ||
B、若上述过程中产生的氧气为1mol,则消耗的H2CrO4为
| ||
| C、上述过程中Cr(OH)3是反应物 | ||
| D、上述过程的氧化产物为H2CrO4 |
c(H+)相等的盐酸和醋酸溶液都稀释相同的倍数后,pH的大小关系是( )
| A、盐酸>醋酸 | B、醋酸>盐酸 |
| C、盐酸=醋酸 | D、无法判断 |
将2.4mol某金属投入1.8L 2mol/L的某酸溶液中,恰好完全反应,并产生7.2g氢气,则该金属和酸分别是( )
| A、二价金属,二元酸 |
| B、二价金属,三元酸 |
| C、三价金属,二元酸 |
| D、一价金属,一元酸 |
在一恒容的密闭容器中,A(g)+B(g)?C(g)的平衡体系中,若增大A的浓度而使平衡向右移动,当达到新的平衡时,则下列说法不正确的是( )
| A、A的平衡浓度一定比原来平衡时大 |
| B、B的平衡浓度一定比原来平衡时小 |
| C、C的百分含量可能比原来平衡时大 |
| D、A的转化率一定比原来平衡时大 |