题目内容
11.铜与浓硫酸反应结束后,烧瓶中铜片未完全溶解.若向反应后的溶液中加入下列物质,相关推断错误的是( )| A. | 加入铁粉,铁粉不溶解 | B. | 滴入NaNO3溶液,铜片不溶解 | ||
| C. | 加入银粉,银粉不溶解 | D. | 滴入NaHCO3溶液,有气体产生 |
分析 A、铁要与铜离子和氢离子发生氧化还原反应,所以铁粉溶解;
B、滴入NaNO3溶液,溶液中的氢离子与硝酸根离子,构成强氧化性体系,与铜片反应;
C、加入银粉,银粉不与铜离子和氢离子反应;
D、碳酸氢钠与未反应的硫酸反应,生成二氧化碳气体.
解答 解:A、铜与浓硫酸反应结束后,浓变稀,溶液中有未反应的硫酸,所以铁要与铜离子和氢离子发生氧化还原反应,则铁粉溶解,故A错误;
B、滴入NaNO3溶液,溶液中的氢离子与硝酸根离子,构成强氧化性体系,与铜片反应,所以铜片溶解,故B错误;
C、加入银粉,银粉不与铜离子和氢离子反应,所以银粉不溶解,故C正确;
D、碳酸氢钠与未反应的硫酸反应,强酸制弱酸,生成二氧化碳气体,故D正确;
故选AB.
点评 本题考查硝酸的化学性质,学生应清楚铜只与浓硫酸反应,不与稀硫酸反应,易错的是B,氢离子与硝酸根离子构成氧化性的体系.

练习册系列答案
相关题目
1.近年来,食品安全事故频繁发生,人们对食品添加剂的认识逐渐加深,Butylated Hydroxy Toluene(简称 BHT)是一种常用的食品抗氧化剂,其合成方法有两种,如图所示:下列说法正确的是( )

| A. |  有五种同分异构体 有五种同分异构体 | B. |  与BHT互为同系物 与BHT互为同系物 | ||
| C. | BHT具有还原性不能发生还原反应 | D. | 两种方法的反应类型都是加成反应 |
2. 如图所示的装置,试管中盛有水,气球a中盛有干燥的Na2O2粉末,U形管中注有浅红色的水.将气球用橡皮绳紧系在试管口.实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象是( )
如图所示的装置,试管中盛有水,气球a中盛有干燥的Na2O2粉末,U形管中注有浅红色的水.将气球用橡皮绳紧系在试管口.实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象是( )
 如图所示的装置,试管中盛有水,气球a中盛有干燥的Na2O2粉末,U形管中注有浅红色的水.将气球用橡皮绳紧系在试管口.实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象是( )
如图所示的装置,试管中盛有水,气球a中盛有干燥的Na2O2粉末,U形管中注有浅红色的水.将气球用橡皮绳紧系在试管口.实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象是( )| A. | U形管内水的红水褪色 | B. | 试管内溶液变红 | ||
| C. | 气球a被吹大 | D. | U形管中水位不变 |
19. 重大节日为保证鲜花盛开,对大量盆栽鲜花施用了S=诱抗素制剂.S-诱抗素的分子结构如图所示.下列关于该物质的说法正确的是( )
重大节日为保证鲜花盛开,对大量盆栽鲜花施用了S=诱抗素制剂.S-诱抗素的分子结构如图所示.下列关于该物质的说法正确的是( )
 重大节日为保证鲜花盛开,对大量盆栽鲜花施用了S=诱抗素制剂.S-诱抗素的分子结构如图所示.下列关于该物质的说法正确的是( )
重大节日为保证鲜花盛开,对大量盆栽鲜花施用了S=诱抗素制剂.S-诱抗素的分子结构如图所示.下列关于该物质的说法正确的是( )| A. | 该有机物的分子式为C15H22O4 | |
| B. | 1mol该有机物与足量Na反应生成1molH2 | |
| C. | 该有机物能发生取代、加成和水解反应 | |
| D. | 1mol该有机物与足量溴反应最多消耗4molBr2 |
6.以石墨为电极分别电解水和饱和食盐水,关于两个电解池反应的说法正确的是( )
| A. | 阳极反应式相同 | |
| B. | 电解结束后所得液体的pH相同 | |
| C. | 阴极反应式相同 | |
| D. | 通过相同电量时生成的气体总体积相等(同温同压) |
3.用下列实验装置室温下进行相应实验,能达到实验目的是( )
| A. | 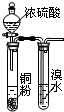 验证浓硫酸具有强氧化性 | B. |  制取干燥的NH3 | ||
| C. |  干燥、收集并吸收多余SO2 | D. | 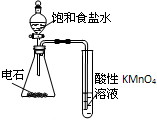 验证乙炔的还原性 |
20.部分弱电解质的电离平衡常数如下表,以下选项错误的是( )
| 化学式 | NH3•H2O | CH3COOH | HCN | H2CO3 |
| Ki(25℃) | 1.8×l0-5 | 1.8×l0-5 | 4.9×l0-10 | Ki1=4.3×l0-7 Ki2=5.6×l0-11 |
| A. | 等物质的量浓度的NaHCO3和NaCN溶液,前者溶液中水的电离程度大 | |
| B. | 0.1 mol/L CH3COONa 溶液显碱性,0.1 mol/L CH3COONH4 溶液显中性 | |
| C. | CN-+H2O+CO2→HCN+HCO3- | |
| D. | 中和等体积、等pH的CH3COOH和HCN消耗NaOH的量前者小于后者 |
1.用下列实验装置进行相应实验,能达到实验目的是( )


| A. | 用图1所示装置可收集NO气体 | |
| B. | 用图4装置可证明酸性:H2SO4>H2CO3>H2SiO3 | |
| C. | 用图3所示装置可实现反应:2H2O$\frac{\underline{\;电解\;}}{\;}$O2↑+H2↑ | |
| D. | 用图2所示装置可吸收多余氨气且能防止倒吸 |
