题目内容
12.下列反应中,属于加成反应的是( )| A. | CH3CH2OH+CH3COOH$→_{△}^{催化剂}$ CH3COOCH2CH3+H2O | |
| B. | 2CH3CHO+O2 $→_{△}^{催化剂}$2CH3COOH | |
| C. | CH3-CH=CH2+Br2→CH3-CHBr-CH2Br | |
| D. | 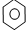 +Br2 $\stackrel{Fe}{→}$ +Br2 $\stackrel{Fe}{→}$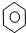 -Br+HBr -Br+HBr |
分析 有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应,据此有机物的结构进行判断.
解答 解:A、乙醇与乙酸反应生成乙酸乙酯属于取代反应,故A错误;
B、乙醛与氧气反应生成乙酸属于氧化反应,故B错误;
C、丙烯与溴反应生成1,2-二溴丙烷,属于加成反应,故C选;
D、苯与液溴在铁催化下生成溴苯,属于取代反应,故D不选,故选C.
点评 本题考查有机反应类型,难度不大,注意掌握有机反应类型概念,侧重学生对基础知识的巩固理解.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
3.下列各组物质中,互为同素异形体的是( )
| A. | 红磷与白磷 | B. | 甲烷与乙烷 | C. | ${\;}_{1}^{1}$H与${\;}_{1}^{2}$H | D. | 正丁烷与异丁烷 |
20.镍镉(Ni-Cd)可充电电池在现代生活中有广泛的应用,它的充放电反应按下式进行:Cd+2NiO(OH)+2H2O$?_{充电}^{放电}$ Cd(OH)2+2Ni(OH)2,该电池放电时的负极材料是( )
| A. | Cd(OH)2 | B. | Ni(OH)2 | C. | NiO(OH) | D. | Cd |
7.下列各组物质,在常温下不发生反应的是( )
①硫化氢和二氧化硫 ②铝与氧化铁 ③铜与稀硝酸 ④石英与纯碱
⑤一氧化氮与氧气 ⑥硅与氧气.
①硫化氢和二氧化硫 ②铝与氧化铁 ③铜与稀硝酸 ④石英与纯碱
⑤一氧化氮与氧气 ⑥硅与氧气.
| A. | ②③⑤ | B. | ②④⑥ | C. | ①②⑥ | D. | ①③⑤ |
17.下列说法正确的是( )
| A. | 若2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ•mol-1,则H2燃烧热为241.8 kJ•mol-1 | |
| B. | 原子弹爆炸是放热反应 | |
| C. | 若C(石墨,s)=C(金刚石,s)△H>0,则石墨能量低且键能小 | |
| D. | 由BaSO4(s)+4C(s)=4CO(g)+BaS(s)△H1=+571.2kJ•mol-1①BaSO4(s)+2C(s)=2CO2(g)+BaS(s)△H2=+226.2kJ•mol-1 ②可得反应C(s)+CO2(g)=2CO(g) 的△H=+172.5kJ•mol-1 |
4.金属铜的提炼多从黄铜矿开始.黄铜矿的焙烧过程中主要反应之一的化学方程式为:2CuFeS2+O2═□+2FeS+SO2,下列说法不正确的是( )
| A. | 方框中的物质应为 Cu2S | |
| B. | 若有1 molSO2生成,则反应中有4 mol 电子转移 | |
| C. | SO2既是氧化产物又是还原产物 | |
| D. | O2只作氧化剂 |
3.今有氢、氧、氮、钠、钙、氟、氯、铜8种元素.
(1)铜位于周期表 周期第四周期ⅠB族.
(2)用“>”、“<”填写下表
(3)已知下列共价键键能数据:
写出氧气与氯化氢气体反应生成氯气和气态水的热化学方程式:O2(g)+4HCl(g)=2Cl2(g)+2H2O(g)△H=-116KJ/mol.
(4)铜能与浓盐酸缓慢发生置换反应,有配合物H[CuCl2]生成.
①该反应的化学方程式为2Cu+4HCl(浓)=2H[CuCl2]+H2↑.
②H[CuCl2]在空气中久置会生成含[Cu(H2O)4]2+的蓝色溶液,[Cu(H2O)4]2+的结构可用示意图表示为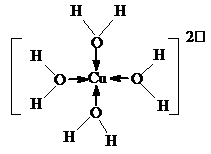 .
.
(1)铜位于周期表 周期第四周期ⅠB族.
(2)用“>”、“<”填写下表
| 第一电离能 | 电负性 | 晶格能 | 沸点 |
| O<N | Cl<F | NaCl<CaO | HF>HCl |
| 共价键 | H-Cl | O=O | H-O | Cl-Cl |
| 键能/kJ•mol-1 | 431 | 498 | 463 | 243 |
(4)铜能与浓盐酸缓慢发生置换反应,有配合物H[CuCl2]生成.
①该反应的化学方程式为2Cu+4HCl(浓)=2H[CuCl2]+H2↑.
②H[CuCl2]在空气中久置会生成含[Cu(H2O)4]2+的蓝色溶液,[Cu(H2O)4]2+的结构可用示意图表示为
 .
.