题目内容
13.向50mL 0.018mol•L-1 AgNO3溶液中加入50mL 0.020mol•L-1的盐酸,生成沉淀,如果溶液中c(Ag+),c(Cl-)的乘积是一个常数:c(Ag+)•c(Cl-)=1.0×10-10,(mol•L-1)2,试求:(1)沉淀生成后溶液中c(Ag+)为1.0×10-7mol/L;
(2)沉淀生成后的溶液的pH是2.
分析 (1)依据题干数据计算沉淀后溶液中氯离子浓度,结合Ksp计算溶液中银离子浓度;
(2)沉淀后溶液中剩余氢离子浓度,计算pH.
解答 解:(1)向50ml0.018mol/L的AgNO3溶液中加入50ml0.02mol/L的盐酸,混合后两者浓度分别为c(Ag+)=$\frac{0.018}{2}$mol/L=0.009 mol/L、c(Cl-)=$\frac{0.02}{2}$mol/L=0.01mol/L,Ag+与Cl-是等物质的量反应的,此时Cl-过量,过量浓度c(Cl-)=0.01mol/L-0.009mol/L=0.001mol/L,
Ksp=c(Ag+)×C(Cl-)=1.0×10-10,则:c(Ag+)=$\frac{1.0×1{0}^{-10}}{0.001}$mol/L=1.0×10-7mol/L,
故答案为:1.0×10-7mol/L;
(2)沉淀生成后,氢离子浓度c=$\frac{0.02mol/L}{2}$=0.01mol/L,所以pH=2,
故答案为:2.
点评 本题考查溶液浓度的计算,侧重于学生的分析、计算能力的考查,为高频考点,本题难度不大,做题时注意判断两种物质的反应程度,再根据溶度积常数计算.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
4.某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1:2,下列说法正确的是( )
| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:4 | ||
| C. | 分子中可能含有氧原子 | D. | 此有机物的最简式为CH4 |
1.已知25℃时:
在无机化合物的提纯中,常利用难溶电解质的沉淀溶解平衡原理除去某些离子.例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,加入一定量的试剂反应,过滤结晶.
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的Mg(OH)2,充分反应,过滤结晶.
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶.请回答下列问题:
(1)下列与方案③相关的叙述中,正确的是ACD(填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或氧化铜
D.在pH>4的溶液中Fe3+一定不能大量存在
(2)方案③中,当Fe3+全沉淀时,溶液中c(Cu2+)的范围为≤2.2mol/L.
| 电解质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶度积(Ksp) | 2.2×10-20 | 8.0×10-15 | 4.0×10-38 |
| 完全沉淀时的pH | ≥5.0 | ≥5.5 | ≥4.0 |
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,加入一定量的试剂反应,过滤结晶.
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的Mg(OH)2,充分反应,过滤结晶.
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶.请回答下列问题:
(1)下列与方案③相关的叙述中,正确的是ACD(填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或氧化铜
D.在pH>4的溶液中Fe3+一定不能大量存在
(2)方案③中,当Fe3+全沉淀时,溶液中c(Cu2+)的范围为≤2.2mol/L.
5.为了使0.1mol•L-1 Na2CO3溶液中c(CO32-)接近0.1mol•L-1,应采取( )
| A. | 加入少量的碳酸钠固体 | B. | 通入CO2 | ||
| C. | 加入少量盐酸 | D. | 加入少量氢氧化钙固体 |
12.下列有关海水综合利用的说法正确的是( )
| A. | 利用电解的方法可以从海水中获取淡水 | |
| B. | 海水蒸发制海盐的过程只发生了化学变化 | |
| C. | 海水中含有钾元素,只需经过物理变化可以得到钾单质 | |
| D. | 从海水中可以得到NaCl,电解熔融NaCl可制备Na |
9.下列氢氧化物中,碱性最强的是( )
| A. | Ca(OH)2 | B. | NaOH | C. | KOH | D. | Al(OH)3 |
10.下列除去杂质的方法正确的是( )
| 物质 | 杂质 | 试剂 | 主要操作 | |
| A | Fe2O3 | SiO2 | NaOH | 过滤 |
| B | CO2 | CO | O2 | 点燃 |
| C | FeCl2溶液 | FeCl3 | Cu | 分液 |
| D | CH3CH2OH | H2O | Na | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
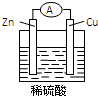 Zn-Cu-H2SO4原电池的负极材料是Zn,正极反应式是2H++2e-═H2↑,发生还原反应反应(填反应类型),总反应式为Zn+H2SO4═ZnSO4+H2↑.
Zn-Cu-H2SO4原电池的负极材料是Zn,正极反应式是2H++2e-═H2↑,发生还原反应反应(填反应类型),总反应式为Zn+H2SO4═ZnSO4+H2↑.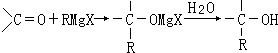

 ,
,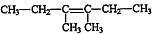 ;
;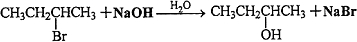 ,I→J
,I→J .
.