题目内容
15.化学与生化、社会密切相关,下列说法不正确的是( )| A. | 维生素在天然食品中含量丰富,所以加工后的食品中维生素的含量也高 | |
| B. | 2M+N=2P+2Q,2P+M=Q(M、N为原料,Q为期望产品)符合“化学反应的绿色化”的要求 | |
| C. | 稀的双氧水可用于清洗伤口,以达到杀菌、消毒的目的 | |
| D. | 可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
分析 A.维生素易被氧化;
B.绿色化学即对环境友好型化学,要求原料物质中所有的原子完全被利用且全部转入期望的产品中,原子的利用率100%;
C.双氧水有强氧化性;
D.Si3N4、Al2O3熔点高.
解答 解:A.维生素易被氧化,加工后食品维生素含量降低,故A错误;
B.反应物能全部转化为生成物,符合绿色化学,故B正确;
C.双氧水有强氧化性,可以消毒杀菌,故C正确;
D.Si3N4、Al2O3熔点高,可用于制作高温结构陶瓷制品,故D正确.
故选A.
点评 本题考查较为综合,为高考常见题型,侧重于元素化合物知识与生活、生产的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
相关题目
19.下列关于Li、Na、K、Rb、Cs碱金属元素的性质比较中,与事实不完全相符合的是( )
| A. | 原子半径依次增大 | B. | 离子半径依次增大 | ||
| C. | 单质的密度依次逐渐增大 | D. | 氢氧化物的碱性依次增强 |
6.软锰矿的主要成分为MnO2,还含有Fe2O3、MgO、Al2O3、CaO、SiO2等杂质,工业上用软锰矿制取MnSO4•H2O的流程如下:

已知:①部分金属阳离子完全沉淀时的pH如下表
②温度高于27℃时,MnSO4晶体的溶解度随温度的升高而逐渐降低.
(1)“浸出”过程中MnO2转化为Mn2+的离子方程式为SO2+MnO2═Mn2++SO42-;
(2)第1步除杂中加入H2O2的目的是将Fe2+氧化为Fe3+.
(3)第1步除杂中形成滤渣l的主要成分为Al(OH)3、Fe(OH)3(填化学式),调pH至5-6所加的试剂,可选择a、b(填以下试剂的序号字母); a.Cao b.MgO c.Al2O3 d.氨水
(4)第2步除杂,主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Mg2+的离子反应方程式MnF2+Mg2+═Mn2++MgF2,该反应的平衡常数数值为7.2×107.
(已知:MnF2的Ksp=5.3×10-3;CaF2的Ksp=1.5×10-10;MgF2的Ksp=7.4×10-11):
(5)采用“趁热过滤”操作的原因是因为减少MnSO4•H2O在水中的溶解,得到更所得产品.
(6)取少量MnSO4•H2O溶于水,配成溶液,测其pH发现该溶液显酸性,原因是Mn2++2H2O?Mn(OH)2+2H+(用离子方程式表示),该溶液中所有离子的浓度由大到小的顺序为c(SO42-)>c(Mn2+)>c(H+)>c(OH-).

已知:①部分金属阳离子完全沉淀时的pH如下表
| 金属阳离子 | Fe3+ | Al3+ | Mn2+ | Mg2+ |
| 完全沉淀时的PH值 | 3.2 | 5.2 | 10.4 | 12.4 |
(1)“浸出”过程中MnO2转化为Mn2+的离子方程式为SO2+MnO2═Mn2++SO42-;
(2)第1步除杂中加入H2O2的目的是将Fe2+氧化为Fe3+.
(3)第1步除杂中形成滤渣l的主要成分为Al(OH)3、Fe(OH)3(填化学式),调pH至5-6所加的试剂,可选择a、b(填以下试剂的序号字母); a.Cao b.MgO c.Al2O3 d.氨水
(4)第2步除杂,主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Mg2+的离子反应方程式MnF2+Mg2+═Mn2++MgF2,该反应的平衡常数数值为7.2×107.
(已知:MnF2的Ksp=5.3×10-3;CaF2的Ksp=1.5×10-10;MgF2的Ksp=7.4×10-11):
(5)采用“趁热过滤”操作的原因是因为减少MnSO4•H2O在水中的溶解,得到更所得产品.
(6)取少量MnSO4•H2O溶于水,配成溶液,测其pH发现该溶液显酸性,原因是Mn2++2H2O?Mn(OH)2+2H+(用离子方程式表示),该溶液中所有离子的浓度由大到小的顺序为c(SO42-)>c(Mn2+)>c(H+)>c(OH-).
3.下列实验装置或操作设计正确且能达到实验目的是( )
| A. |  称量NaOH固体 | B. |  配制一定物质的量浓度稀硫酸 | ||
| C. |  制取少量的Fe(OH)3胶体 | D. |  用H2SO4标准溶液滴定NaOH溶液 |
10.下列说法正确的是( )
| A. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰钾溶液褪色 | |
| B. | 棉、丝、羽毛、塑料及合成橡胶完全燃烧都只生成CO2和H2O | |
| C. | 纤维素、合成纤维、光导纤维都是有机高分子化合物 | |
| D. | 液化石油气可由石油分馏获得,汽油可由石油分馏或石油裂化获得 |
20.已知A、B、C、D、E是短周期中原子序数依次增大的5中主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 1mol由元素A、B组成的化合物一定含有18mole- | |
| B. | 化合物AE与DE3有相同类型的化学键 | |
| C. | 工业上常用电解法制备元素C、D、E的单质 | |
| D. | 元素D的最高价氧化物对应的水化物可以溶于过量的氨水中 |
7.由下列实验现象得出的结论正确的是( )
| 选项 | 实验现象 | 结论 |
| A | 取某Na2SO3溶液,加入足量的稀盐酸,产生气泡,再滴加BaCl2溶液,产生白色沉淀. | Na2SO3已部分被氧化 |
| B | 向2mL0.1mol/LNaOH溶液中滴加0.1mol/LMgCl2溶液3滴,出现白色沉淀后,再滴加3滴0.1mol/L FeCl3溶液,出现红褐色沉淀. | 溶解度:Mg(OH)2>Fe(OH)3 |
| C | 向氯水中通入足量SO2,氯水褪色. | SO2具有漂白性 |
| D | 相同温度下,测等浓度的Na2CO3和Na2SO3水溶液的pH:pH (Na2CO3)>pH(Na2SO3). | 非金属性强弱:C>S |
| A. | A | B. | B | C. | C | D. | D |
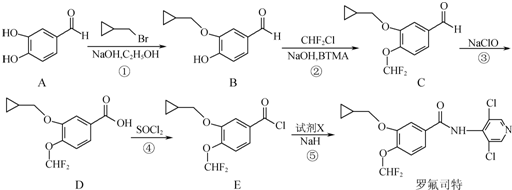
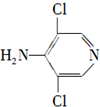 .
.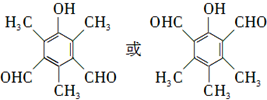 等.
等.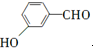 、CH3CH2OH为原料制备
、CH3CH2OH为原料制备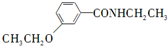 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下: