题目内容
10.下列说法正确的是( )| A. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰钾溶液褪色 | |
| B. | 棉、丝、羽毛、塑料及合成橡胶完全燃烧都只生成CO2和H2O | |
| C. | 纤维素、合成纤维、光导纤维都是有机高分子化合物 | |
| D. | 液化石油气可由石油分馏获得,汽油可由石油分馏或石油裂化获得 |
分析 A.聚乙烯中不含碳碳双键;
B.棉的成分为纤维素,丝、羽毛的成分为蛋白质;
C.光导纤维的成分为二氧化硅;
D.汽油中主要含烯烃,石油分馏可得到液化石油气和汽油等.
解答 解:A.聚乙烯中不含碳碳双键,不能使酸性高锰钾溶液褪色,而乙烯、氯乙烯均可使酸性高锰钾溶液褪色,故A错误;
B.丝、羽毛的成分为蛋白质,燃烧产物除CO2和H2O,还有氮气,故B错误;
C.光导纤维的成分为二氧化硅,不属于有机物,而纤维素、合成纤维都是有机高分子化合物,故C错误;
D.汽油中主要含烯烃,石油分馏可得到液化石油气和汽油等,石油裂化得到烯烃类有机物,则液化石油气可由石油分馏获得,汽油可由石油分馏或石油裂化获得,故D正确;故选D.
点评 本题考查较综合,涉及物质的组成、性质及石油产品,侧重有机物结构、有机反应及石油裂化的考查,注重基础知识的夯实,题目难度不大.

练习册系列答案
相关题目
14.下列说法中,正确的是( )
| A. | SO2水溶液能导电,所以SO2是电解质 | |
| B. | NaCl溶液能导电所以NaCl溶液是电解质 | |
| C. | 向醋酸溶液中加入少量氢氧化钠固体,溶液的导电能力降低 | |
| D. | Na2CO3既是钠盐又是碳酸盐 |
1.某化学小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备NiSO4•7H2O.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).

部分阳离子以氢氧化物形式沉淀时的pH如下:
(1)“碱浸”过程中发生反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑、Al2O3+2OH-=2AlO2-+3H2O.
(2)“酸浸”时所加入的酸是H2SO4 (填化学式);酸浸后,经操作a分离出固体①后,溶液中可能含有的金属离子是Ni2+、Fe2+、Fe3+.
(3)加入H2O2时发生反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(4)操作b为调节溶液的pH,你认为pH的调控范围是3.2-7.1.
(5)产品晶体中有时会混有少量绿矾(FeSO4•7H2O),其原因可能是H2O2的用量不足(或H2O2失效)、保温时间不足导致Fe2+未被完全氧化造成的(写出一点即可).
(6)NiS04•7H20可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M=NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-.
(7)一般认为残留在溶液中的离子浓度小于1×10-5 mol/L时,沉淀已经完全.请利用上表中数据,估算Fe(OH)2的溶度积常数1×10-13.6(mol/L)3,和可逆反应Fe2++2H2O=2H++Fe(OH)2 在25℃时的平衡常数1×10-14.4(mol/L).

部分阳离子以氢氧化物形式沉淀时的pH如下:
| 沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ai(OH)2 | 7.1 | 9.2 |
(2)“酸浸”时所加入的酸是H2SO4 (填化学式);酸浸后,经操作a分离出固体①后,溶液中可能含有的金属离子是Ni2+、Fe2+、Fe3+.
(3)加入H2O2时发生反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(4)操作b为调节溶液的pH,你认为pH的调控范围是3.2-7.1.
(5)产品晶体中有时会混有少量绿矾(FeSO4•7H2O),其原因可能是H2O2的用量不足(或H2O2失效)、保温时间不足导致Fe2+未被完全氧化造成的(写出一点即可).
(6)NiS04•7H20可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M=NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH-.
(7)一般认为残留在溶液中的离子浓度小于1×10-5 mol/L时,沉淀已经完全.请利用上表中数据,估算Fe(OH)2的溶度积常数1×10-13.6(mol/L)3,和可逆反应Fe2++2H2O=2H++Fe(OH)2 在25℃时的平衡常数1×10-14.4(mol/L).
5.如图为截取的元素周期表前4周期的一部分,且X、Y、Z、R和W均为主族元素,下列说法正确的是( )
| X | ||
| Y | Z | R |
| W |
| A. | Z的氧化物与X单质不可能发生置换反应 | |
| B. | 五种元素的原子最外层电子数一定都大于2 | |
| C. | X、Z原子序数可能相差18 | |
| D. | Z可能是氯元素 |
15.化学与生化、社会密切相关,下列说法不正确的是( )
| A. | 维生素在天然食品中含量丰富,所以加工后的食品中维生素的含量也高 | |
| B. | 2M+N=2P+2Q,2P+M=Q(M、N为原料,Q为期望产品)符合“化学反应的绿色化”的要求 | |
| C. | 稀的双氧水可用于清洗伤口,以达到杀菌、消毒的目的 | |
| D. | 可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
2.化学与生活、社会密切相关,下列说法错误的是( )
| A. | 玻璃属于无机非金属材料 | B. | 煤的气化属于物理变化 | ||
| C. | 雾霾与汽车尾气的排放有关 | D. | 甲醛的水溶液可以用来浸泡标本 |
19.下列图示与对应的叙述相符的是( )


| A. | 图1表示相同温度下,相同体积、pH均为1的盐酸和醋酸溶液分别加水稀释时溶液pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 | |
| B. | 图2表示CH3COOH溶液中逐步加CH3COONa固体后,溶液pH的变化 | |
| C. | 图3表示某可逆反应正、逆反应速率随温度变化,则该反应的正反应是吸热反应 | |
| D. | 图4表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)???N2O4(g),相同时间后测得NO2体积分数的曲线,则该反应的正反应△H<0 |
 .
.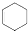 的六元环结构,六元环上只有一个取代基
的六元环结构,六元环上只有一个取代基