题目内容
20.在平面形分子ClCH=CHCl中,C-Cl键采用的成键轨道是( )| A. | sp-s | B. | sp2-s | C. | sp2-p | D. | sp3-s |
分析 在平面形分子ClCH=CHCl中,每个C原子含有3个σ键和1个π键,所以价层电子对个数是3,采用sp2杂化,Cl原子中未成对电子为3p电子,据此判断C-Cl键采用的成键轨道.
解答 解:在平面形分子ClCH=CHCl中,每个C原子含有3个σ键和1个π键,所以价层电子对个数是3,采用sp2杂化,Cl原子中未成对电子为3p电子,所以C-Cl键采用的成键轨道是sp2-p,故选C.
点评 本题考查原子轨道杂化,为高频考点,根据价层电子对互斥理论确定原子杂化类型,熟悉常见原子结构及原子核外电子排布、价层电子对个数的计算方法,题目难度不大.

练习册系列答案
相关题目
1.下列有关叙述合理的是( )
| A. | 向澄清石灰水中加入少许NaOH固体,溶液不出现浑浊 | |
| B. | 向饱和Na2CO3溶液中通入CO2气体,一定有浑浊 | |
| C. | 向大量饱和CuSO4溶液中加入16gCuSO4,保持温度不变,析出晶体质量25g | |
| D. | 大量MnO2与含4mol HCl的浓盐酸共热,充分反应后生成Cl2的物质的量小于1mol |
8.将amol纯铁粉投入含HNO3bmol的稀溶液里,恰好完全反应并放出NO气体,则a和b的关系是( )
| A. | $\frac{a}{b}$=$\frac{1}{4}$ | B. | $\frac{a}{b}$=$\frac{3}{8}$ | C. | $\frac{1}{4}$≤$\frac{a}{b}$≤$\frac{3}{8}$ | D. | $\frac{a}{b}$的值无法确定 |
15.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | MgO的熔点很高,可用于制作耐高温材料 | |
| D. | 电解AlCl3饱和溶液,可制得金属铝 |
12.某高分子材料的结构如图所示: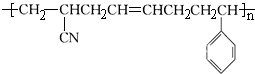 ,以下与此高分子材料相关的说法正确的是( )
,以下与此高分子材料相关的说法正确的是( )
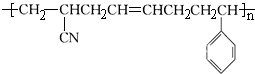 ,以下与此高分子材料相关的说法正确的是( )
,以下与此高分子材料相关的说法正确的是( )| A. | 合成该高分子材料的反应是缩聚反应 | |
| B. | 该高分子材料是由三种单体聚合而成的 | |
| C. | 合成该高分子材料的部分单体不能使溴水和酸性高锰酸钾溶液褪色 | |
| D. | 该高分子材料是体型结构高分子,具有热固性 |
 .
.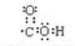 ;
; 反应类型:加聚反应.
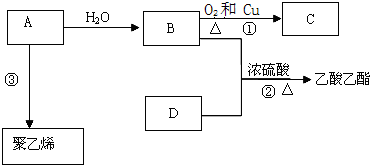
反应类型:加聚反应.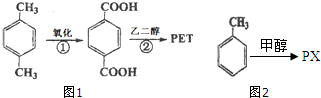 对二甲苯(英文名称p-xylene,缩写为PX)是一种低毒化合物,也是聚酯工业的重要原料,主要用于生产对苯二甲酸(PTA),对苯二甲酸再和乙二醇(EG)反应生成聚对苯二甲酸乙二醇酯(PET).国内对二甲苯产量增长步伐放缓,供应缺口加大,近一半的PX依靠进口.以PX为主要原料生产PET的一种路线如图1:
对二甲苯(英文名称p-xylene,缩写为PX)是一种低毒化合物,也是聚酯工业的重要原料,主要用于生产对苯二甲酸(PTA),对苯二甲酸再和乙二醇(EG)反应生成聚对苯二甲酸乙二醇酯(PET).国内对二甲苯产量增长步伐放缓,供应缺口加大,近一半的PX依靠进口.以PX为主要原料生产PET的一种路线如图1: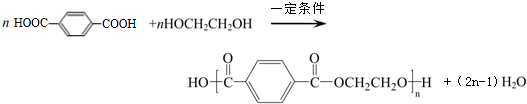 .(不用注明条件)
.(不用注明条件)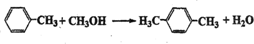 .(不用注明条件)
.(不用注明条件)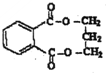 .
.