题目内容
【题目】完成下列各问题:
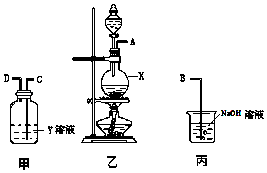
(1)①泡沫灭火器中的药品为NaHCO3和Al2(SO4)3,其反应的离子方程式为:__________;
②TiCl4水解生成TiO2·xH2O的化学方程式__________;
③酸性高锰酸钾溶液与草酸溶液反应的化学方程式____________;
④硫代硫酸钠溶液与稀硫酸反应的化学万式____________;
(2)碳酸氢钠溶液中的粒子物质的量浓度有多种关系,请分别写出
①电荷数守恒_________;
②物料守恒___________;
③质子守恒___________;
④下列粒子浓度由大到小的顺序为c(Na+)、c(HCO3-)、c(CO32-),c(H2CO3)、c(OH-)_________。
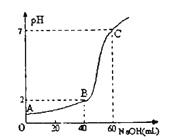
(3)常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示。所用NaOH溶液浓度为____________。
【答案】 3HCO3-+Al3+=Al(OH)3↓+3CO2↑ TiCl4+(2x+2)H2O![]() TiO2·xH2O+4HCl 5H2C2O4+2KMnO4+3H2SO4=10CO2↑+2MnSO4+K2SO4+8H2O Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) c(H+)+c(H2CO3)= c(OH-)+c(CO32-) c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>C(CO32-) 0.03mo1/L
TiO2·xH2O+4HCl 5H2C2O4+2KMnO4+3H2SO4=10CO2↑+2MnSO4+K2SO4+8H2O Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) c(H+)+c(H2CO3)= c(OH-)+c(CO32-) c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>C(CO32-) 0.03mo1/L
【解析】(1)①泡沫灭火器中的药品为NaHCO3和Al2(SO4)3,HCO3-和Al3+均可发生水解,且相互促进,产生气体CO2和沉淀Al(OH)3,其反应的离子方程式为:3HCO3-+Al3+=Al(OH)3↓+3CO2↑ ;②TiCl4水解生成TiO2·xH2O,设TiCl4的系数为1,根据元素守恒,TiO2·xH2O的系数为1,HCl的系数为4;再根据O元素守恒,可知H2O的系数为(2+x),化学方程式TiCl4+(2x+2)H2O![]() TiO2·xH2O+4HCl ;③酸性溶液KMnO4与草酸发生氧化还原反应,KMnO4→MnSO4,Mn元素的化合价从+7价降低到+2价得到5个电子,被还原,得到还原产物MnSO4,H2C2O4→2CO2中C元素升高失去2个电子,被氧化得到氧化产物CO2,根据得失电子守恒,KMnO4与H2C2O4,的计量数之比为2:5,再根据原子守恒平衡酸性高锰酸钾溶液与草酸溶液反应的化学方程式5H2C2O4+2KMnO4+3H2SO4=10CO2↑+2MnSO4+K2SO4+8H2O ;④硫代硫酸钠遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,硫代硫酸钠溶液与稀硫酸反应的化学万式Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O;(2)碳酸氢钠溶液中的粒子物质的量浓度有多种关系,请分别写出①电荷数守恒c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-);②物料守恒c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) ;③将②代入①,消去c(Na+),得质子守恒c(H+)+c(H2CO3)= c(OH-)+c(CO32-);④NaHCO3溶液中HCO3-水解程度大于电离程度导致溶液呈碱性,则c(CO32-)<c(H2CO3),c(Na+)不水解,浓度最大,下列粒子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>C(CO32-);(3)设HCl的浓度是x mol·L-1,NaOH溶液浓度为y mol·L-1,结合图象则有:①20×10-3L×x mol·L-1=60×10-3L×y mol·L-1,②20×10-3L×x mol·L-1-40×10-3L×y mol·L-1=0.01 mol·L-1×(20+40)×10-3L,根据①②解得:x=0.09mol·L-1,y=0.03mol·L-1,即HCl的浓度是0.09mol·L-1,NaOH溶液浓度为0.03mol·L-1。
TiO2·xH2O+4HCl ;③酸性溶液KMnO4与草酸发生氧化还原反应,KMnO4→MnSO4,Mn元素的化合价从+7价降低到+2价得到5个电子,被还原,得到还原产物MnSO4,H2C2O4→2CO2中C元素升高失去2个电子,被氧化得到氧化产物CO2,根据得失电子守恒,KMnO4与H2C2O4,的计量数之比为2:5,再根据原子守恒平衡酸性高锰酸钾溶液与草酸溶液反应的化学方程式5H2C2O4+2KMnO4+3H2SO4=10CO2↑+2MnSO4+K2SO4+8H2O ;④硫代硫酸钠遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,硫代硫酸钠溶液与稀硫酸反应的化学万式Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O;(2)碳酸氢钠溶液中的粒子物质的量浓度有多种关系,请分别写出①电荷数守恒c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-);②物料守恒c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) ;③将②代入①,消去c(Na+),得质子守恒c(H+)+c(H2CO3)= c(OH-)+c(CO32-);④NaHCO3溶液中HCO3-水解程度大于电离程度导致溶液呈碱性,则c(CO32-)<c(H2CO3),c(Na+)不水解,浓度最大,下列粒子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>C(CO32-);(3)设HCl的浓度是x mol·L-1,NaOH溶液浓度为y mol·L-1,结合图象则有:①20×10-3L×x mol·L-1=60×10-3L×y mol·L-1,②20×10-3L×x mol·L-1-40×10-3L×y mol·L-1=0.01 mol·L-1×(20+40)×10-3L,根据①②解得:x=0.09mol·L-1,y=0.03mol·L-1,即HCl的浓度是0.09mol·L-1,NaOH溶液浓度为0.03mol·L-1。

【题目】某化学反应2AB+D在三种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如表所示,表中温度为摄氏度(℃).
实验 | 浓度 时间 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | c1 | 0.50 |
2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | T3 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,回答下列问题:
(1)在实验1中,以反应物A浓度的变化表示该反应在0~10min内的平均反应速率为
(2)在实验1中,c1数值为
(3)在实验1、2中有一个实验使用了正催化剂.判断是实验(选填“1”或“2”)使用了正催化剂.
(4)在实验1、3中反应温度不同.判断T3800(选填“<”或“>”).