题目内容
18.实验室可用下列方法制取气体,其中必须用排水法的是( )| A. | 铜片与稀硝酸共热 | B. | 二氧化锰与盐酸共热 | ||
| C. | 锌与稀硫酸共热 | D. | 稀盐酸与碳酸钙的反应 |
分析 能够在空气中稳定存在并且密度明显大于空气的气体或小于空气的气体可以用排空气集气法收集,与水不发生化学反应,并且溶解度不大的气体可以用排水发收集.
解答 解:A.铜片与稀硝酸共热生成一氧化氮,一氧化氮能和空气中的氧气发生生成二氧化氮,即一氧化氮不能在空气中稳定存在,所以不能用排空气集气法收集;一氧化氮不易溶于水,和水不反应,所以能用排水集气法收集,故A正确;
B.二氧化锰与盐酸共热生成氯气,氯气在空气中能稳定存在且密度明显大于空气的密度,所以可用排空气集气法收集,故B错误;
C.锌与稀硫酸共热生成氢气,氢气在空气中能稳定存在且密度明显小于空气的密度,所以可用排空气集气法收集;氢气不易溶于水,和水不发生化学反应,所以可用排水法收集,故C错误;
D.稀盐酸与碳酸钙的反应反应生成二氧化碳,二氧化碳在空气中能稳定存在且密度明显大于空气的密度,所以可用排空气集气法收集;二氧化碳能和水反应生成碳酸,溶解度较大,所以不能用排水法收集,故D错误.
故选A.
点评 本题考查了气体的收集方法的选取,难度不大,根据气体的性质和溶解性确定收集方法即可.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
9.下列有关化学用语正确的是( )
| A. | 乙醇、乙二醇、丙三醇互为同系物,同系物之间不可能互为同分异构体 | |
| B. | 液化石油气和天然气的主要成分都是甲烷 | |
| C. | (CH3)2C=CHCH2CH3分子中的六个碳原子中至少有五个在同一个平面上 | |
| D. | 苯分子的比例模型: |
3.某元素原子的最外层上的电子数是次外层上的电子数的a倍(a>1),则该元素原子核内的质子数为( )
| A. | 2a | B. | 2a+2 | C. | 2a+10 | D. | a+2 |
7.下列过程中,共价键被破坏的是( )
| A. | 溴挥发 | B. | 氯气被木炭吸附 | C. | 食盐溶于水 | D. | 硫酸溶于水 |
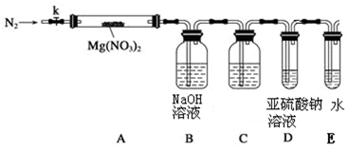 某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.
某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律.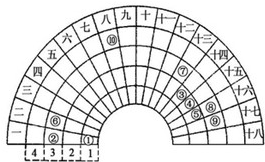 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,请回答下列问题
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,请回答下列问题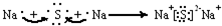
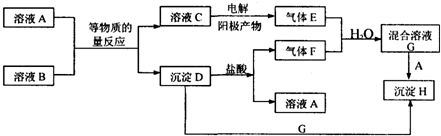
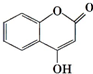 可用来制备抗凝血药,通过下列路线合成:
可用来制备抗凝血药,通过下列路线合成: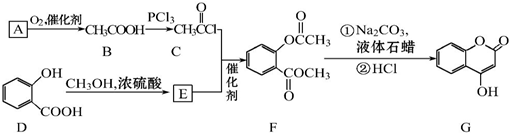
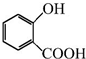 +CH3OH$?_{△}^{浓硫酸}$
+CH3OH$?_{△}^{浓硫酸}$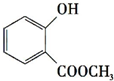 +H2O.
+H2O.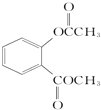 +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+CH3OH+H2O.
+CH3COONa+CH3OH+H2O.