题目内容
1.图中 A、B、C、D、E均为有机化合物.已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物.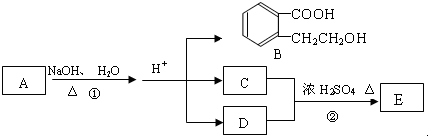
根据上图回答问题:
(1)已知E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,其余为氧,则E的分子式为C5H10O2;D分子中的官能团名称是羟基.
(2)反应②的化学方程式是CH3COOH+CH3CH2CH2OH $→_{△}^{浓硫酸}$CH3COOCH2CH2CH3+H2O.
(3)B发生缩聚反应的化学方程式是
 .(不用写条件)
.(不用写条件)(4)A的结构简式是
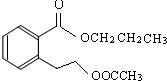 .
.(5)B的同分异构体中有一种同时符合下列三个条件的,其结构简式为:
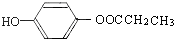 .
.Ⅰ.与 FeCl3 溶液发生显色反应
Ⅱ.苯环上除了有两个取代基,还有两种氢原子
Ⅲ.1mol该物质最多可以与3molNaOH反应.
分析 E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,则碳原子数目为$\frac{102×58.8%}{12}$=5,H原子数目为$\frac{102×9.8%}{1}$=10,氧原子数目=$\frac{102-12×5-10}{16}$=2,则E的分子式为C5H10O2,E由C和D反应生成,C能和碳酸氢钠反应,则C为羧酸,D为醇,二者共含5个C原子,并且C和D的相对分子质量相等,则C为乙酸、D为丙醇,E无支链,D应为1-丙醇,E为CH3COOCHCH2CH3,A在碱性条件下水解,再酸化得B、C、D,所以A是由B与乙酸、丙醇发生酯化反应后生成的产物,其结构简式为: ,据此解答.
,据此解答.
解答 解:E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,则碳原子数目为$\frac{102×58.8%}{12}$=5,H原子数目为$\frac{102×9.8%}{1}$=10,氧原子数目=$\frac{102-12×5-10}{16}$=2,则E的分子式为C5H10O2,E由C和D反应生成,C能和碳酸氢钠反应,则C为羧酸,D为醇,二者共含5个C原子,并且C和D的相对分子质量相等,则C为乙酸、D为丙醇,E无支链,D应为1-丙醇,E为CH3COOCHCH2CH3,A在碱性条件下水解,再酸化得B、C、D,所以A是由B与乙酸、丙醇发生酯化反应后生成的产物,其结构简式为: ,
,
(1)通过以上分析知,E的分子式为:C5H10O2,D为1-丙醇,含有的官能团为羟基,
故答案为:C5H10O2;羟基;
(2)②为乙酸和丙醇的酯化反应,反应方程式为:CH3COOH+CH3CH2CH2OH $→_{△}^{浓硫酸}$CH3COOCH2CH2CH3+H2O,
故答案为:CH3COOH+CH3CH2CH2OH $→_{△}^{浓硫酸}$CH3COOCH2CH2CH3+H2O;
(3)B发生缩聚反应的化学方程式是 ,
,
故答案为: ;
;
(4)由上述分析可知,A为 ,
,
故答案为: ;
;
(5)B的同分异构体符合下列条件:Ⅰ.与 FeCl3 溶液发生显色反应含有间二取代苯环结构,Ⅱ.苯环上除了有两个取代基,还有两种氢原子,Ⅲ.1mol该物质最多可以与3molNaOH反应,符合条件的同分异构体为: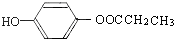 ,
,
故答案为: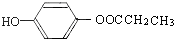 .
.
点评 本题考查有机物的推断,结合反应条件与转化关系,采用正推或逆推的方式进行推断,需要学生熟练掌握官能团性质与转化,难度中等.

 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案| A. | 常温常压下,1mol固体氢氧化钠的体积比1mol氢气的体积小 | |
| B. | NA个氧气分子和NA个氢气分子的质量比为16:l | |
| C. | 28g氮气所含的原子数目为NA | |
| D. | NA个H2SO4分子中所含氧原子个数与4NA个H2O分子中所含氧原子个数相等 |
| A. | CH3OH | B. | C2H5OH | C. | (CH3)3COH | D. | (CH3)3CCH2OH |
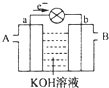 如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )
如图是一氧化碳空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中,正确的是( )| A. | a电极发生还原反应,b电极发生氧化反应 | |
| B. | a电极的电极反应式为:CO+4OH-+2e-=CO2+2H2O | |
| C. | A处通入的是空气,B处通入的是CO | |
| D. | 用这种电池作电源精炼铜,若阴极质量增加6.4 g,则至少消耗标准状况下的CO 2.24 L |
| 品名 | 苏打饼干 |
| 配料 | 面料、鲜鸡蛋、精炼食用植物油、白砂糖、奶油、食盐、苏打 |
| 保质期 | 12个月 |
| 生产日期 | 2015年5月15日 |
| A. | 精炼食用植物油能使溴水和酸性KMnO4溶液褪色 | |
| B. | 白砂糖属于二糖,在人体内水解而转化为单糖 | |
| C. | 鲜鸡蛋清遇浓硝酸变为黄色 | |
| D. | 奶油与白砂糖都是高分子化合物 |
| 元素编号 | 元素性质或原子结构 |
| X | 形成的简单阳离子核外无电子 |
| Y | 元素的气态氢化物和它的最高价氧化物对应的水化物能发生化合反应 |
| Z | 元素在周期表的族序数等于周期序数的3倍 |
| T | 同周期元素中形成的简单离子半径最小 |
| A. | 原子半径大小顺序:T>Z>Y>X | |
| B. | 常温下,T的单质与Y的最高价氧化物对应水化物的浓溶液反应生成氢气 | |
| C. | X分别与Y、Z均可形成既含极性键又含非极性键的化合物 | |
| D. | 由X、Y和Z三种元素构成的强电解质,对水电离均起抑制作用 |
| A. | CH3CH2CH2CH3 | B. | 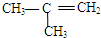 | C. | 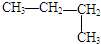 | D. | CH3-CH=CH2 |
| 甲 | ||
| 丁 |
| A. | 简单离子半径:乙>丁 | |
| B. | 乙与氧元素形成的某化合物中可能既有离子键,又有共价键 | |
| C. | 乙、丙、丁三种元素最高价氧化物的水化物两两之间能发生反应 | |
| D. | 甲与丁的核外电子数相差8 |
 短周期元素A、B、C、D在周期表中的位置如图,E2+与D的简单阴离子有相同的电子层结构,回答下列问题:
短周期元素A、B、C、D在周期表中的位置如图,E2+与D的简单阴离子有相同的电子层结构,回答下列问题: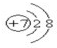 ,元素D位于元素周期表的第ⅥA族.
,元素D位于元素周期表的第ⅥA族.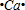 +2
+2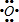 →
→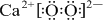 .
.