题目内容
【题目】某小组实验探究葡萄糖、二氧化硫分别与新制氢氧化铜的反应。
实验I新制Cu(OH)2与葡萄糖反应
(1)将1.5mL1.0mol/LCuSO4溶液滴入5mLl.0mol/LNaOH溶液中制得Cu(OH)2悬浊液。相关反应的离子方程式为___________。
(2)在制得的Cu(OH)2悬浊液中加入稍过量葡萄糖溶液,加热煮沸,产生红色沉淀。
①该实验现象说明_______________;
②该原理可用于检测糖尿病患者血液中的______含量。
实验II新制Cu(OH)2与二氧化硫反应
按上述方法重新制取氢氧化铜悬浊液,通入足量二氧化硫,先产生红色沉淀,然后红色沉淀逐渐变为紫红色固体,最终溶液呈无色。
(1)探究红色沉淀转变为紫红色的原因。
将实验I产生的红色沉淀过滤、洗涤,洗涤方法是_____。
将所得固体分成两等份于试管中并加入少量蒸馏水进行对比实验。
实验装置图 |
|
|
操作及现象 | 红色固体很快转变为紫红色固体,溶液呈蓝色。 | 开始红色固体缓慢变为紫红色固体,溶液呈蓝色。试管内紫红色固体逐渐增多,最后溶液变无色。 |
解释及结论 | ①该反应的离子方程式 _________________。 | ②开始时红色固体颜色变化缓慢的原因是_________。 ③所得无色溶液中主要阴离子为___________________。 |
(2)通过上述探究,写出新制氢氧化铜与过量SO2反应的总化学方程式______________。
反思:将表中SO2换为NO2是否能观察到相同现象?回答并解释:__________。
【答案】 Cu2++2OH-=Cu(OH)2↓ Cu(OH)2具有氧化性,葡萄糖具有还原性 葡萄糖 用玻璃棒引流,向过滤器中加入蒸馏水至浸没沉淀,待水流出后,按上述操作重复2~3次 Cu2O+2H+==Cu+Cu2++H2O SO2溶于水后生成的H2SO3酸性比H2SO4弱,c(H+)较小,Cu2O与H+反应慢 SO42- Cu(OH)2+SO2=Cu+H2SO4 不能。因为NO2溶于水生成HNO3具有强氧化性,将Cu2O直接氧化成Cu(NO3)2,溶液呈蓝色,且无紫红色固体生成。
【解析】实验Ⅰ(1)将1.5mL1.0mol/LCuSO4溶液滴入5mLl.0mol/LNaOH溶液中制得Cu(OH)2悬浊液,其方程式为:Cu2++2OH-=Cu(OH)2↓。
(2)①在制得的Cu(OH)2悬浊液中加入稍过量葡萄糖溶液,加热煮沸,产生红色沉淀,说明葡萄糖将氢氧化铜还原为氧化亚铜的红色沉淀,所以说明氢氧化铜有氧化性,葡萄糖有还原性。②这个反应的原理,能利用生成的氧化亚铜沉淀的量,来检测血液中的葡萄糖含量。
实验Ⅱ(1)洗涤沉淀的基本方法就是:向过滤器中加入蒸馏水,使蒸馏水将沉淀表面的杂质洗去,重复操作2~3即可。所以答案为:用玻璃棒引流,向过滤器中加入蒸馏水至浸没沉淀,待水流出后,按上述操作重复2~3次。
①实验中的现象为:红色固体(氧化亚铜)很快转变为紫红色固体(单质铜),溶液呈蓝色(铜离子),所以反应为:Cu2O+2H+==Cu+Cu2++H2O。
②氧化亚铜转化为单质铜和铜离子,需要在酸性条件下进行,而亚硫酸的酸性弱,氢离子较少,所以开始时反应比较慢。
③最后溶液的蓝色褪去,说明铜离子都被二氧化硫还原为单质铜了,所以二氧化硫应该被氧化为硫酸根离子。
(2)由上,新制氢氧化铜与过量SO2反应生成单质铜和硫酸根离子,所以反应为:Cu(OH)2+SO2=Cu+H2SO4。如果将表中SO2换为NO2,NO2与水反应生成具有强氧化性的硝酸,硝酸可以直接将氧化亚铜转化为硝酸铜,所以无法观察到同样的现象。

【题目】I.已知2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是__________________的影响。
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入__________________。
A.硫酸钾 B.硫酸锰 C.氯化钾 D.水
II. 分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题。
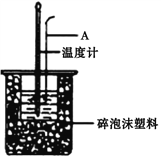
(1)仪器A的名称是__________________,烧杯间填满碎泡沫塑料的作用是__________________。
(2)加入NaOH溶液的正确操作是__________________ (填字母)。
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g·℃)。为了计算中和热,某学生实验记录数据如下:
实验序号 | 起始温度t1℃ | 终止温度t2℃ | |
盐酸 | 氢氧化钠 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热△H=__________________(结果保留一位小数)。
(4)实验中若改用50 mL 0.50 mol/L的盐酸与40 mL 0.55 mol/L的氢氧化钠溶液进行反应, 与上述实验相比,所放出的热量__________________(填“相等”“不相等”),若实验操作均正确,则所求中和热__________________(填“相等”“不相等”)。