题目内容
根据以下实验事实,判断四种微粒在酸性条件下,氧化性由强到弱的顺序是( )
①向FeCl3溶液中滴加KI溶液,再加入CCl4振荡,CCl4层呈紫色;
②向FeCl2溶液中加入氯水,再加入KSCN溶液,呈红色;
③向KMnO4溶液中加入浓盐酸,振荡后紫色褪去.
①向FeCl3溶液中滴加KI溶液,再加入CCl4振荡,CCl4层呈紫色;
②向FeCl2溶液中加入氯水,再加入KSCN溶液,呈红色;
③向KMnO4溶液中加入浓盐酸,振荡后紫色褪去.
| A、I2>Cl2>Fe3+>MnO4- |
| B、MnO4->Cl2>Fe3+>I2 |
| C、Cl2>I2>Fe3+>MnO4- |
| D、Fe3+>MnO4->Cl2>I2 |
考点:氧化性、还原性强弱的比较
专题:氧化还原反应专题
分析:氧化还原反应中 氧化剂的氧化性大于氧化产物,根据化合价判断反应中氧化剂和氧化产物,然后判断.
解答:
解:①FeCl3溶液中滴入KI溶液,加CCl4振荡,CCl4层呈紫色,发生了反应FeCl3+2KI=2FeCl2+I2,氧化剂Fe3+的氧化性大于I2;
②FeCl2溶液中滴加氯水,再加KSCN溶液,呈红色,说明氯气氧化亚铁离子生成铁离子和氯离子,反应为2Fe2++Cl2=2Fe3++2Cl-;反应中氧化剂Cl2氧化性大于氧化产物Fe3+;
③KMnO4溶液中滴加盐酸.KMnO4溶液的紫色褪去,说明高锰酸钾氧化氯离子为氯气,本身被还原为锰离子;反应中氧化剂KMnO4的氧化性大于氧化产物Cl2;
综上所述氧化性强弱为MnO-4>Cl2>Fe3+>I2;
故选B.
②FeCl2溶液中滴加氯水,再加KSCN溶液,呈红色,说明氯气氧化亚铁离子生成铁离子和氯离子,反应为2Fe2++Cl2=2Fe3++2Cl-;反应中氧化剂Cl2氧化性大于氧化产物Fe3+;
③KMnO4溶液中滴加盐酸.KMnO4溶液的紫色褪去,说明高锰酸钾氧化氯离子为氯气,本身被还原为锰离子;反应中氧化剂KMnO4的氧化性大于氧化产物Cl2;
综上所述氧化性强弱为MnO-4>Cl2>Fe3+>I2;
故选B.
点评:本题考查了氧化还原反应的强弱规律应用,掌握基础,概念判断和产物分析是关键,题目难度中等.

练习册系列答案
相关题目
观察如图几个装置示意图,有关叙述正确的是( )
A、装置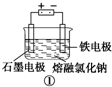 工业上可用于生产金属钠,电解过程中石墨电极产生金属,此法也可用于生产活泼金属镁、铝等 工业上可用于生产金属钠,电解过程中石墨电极产生金属,此法也可用于生产活泼金属镁、铝等 |
B、装置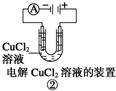 中随着电解的进行左边电极会产生红色的铜,并且电流表示数不断变小 中随着电解的进行左边电极会产生红色的铜,并且电流表示数不断变小 |
C、装置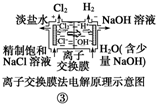 中的离子交换膜只允许阳离子、阴离子和小分子水通过 中的离子交换膜只允许阳离子、阴离子和小分子水通过 |
D、装置 的待镀铁制品应与电源正极相连 的待镀铁制品应与电源正极相连 |
下列有关物质的分类或归类正确的是( )
①混合物:冰醋酸、水玻璃、水银 ②化合物:CaCl2、烧碱、聚乙烯
③电解质:明矾、胆矾、硫酸钡 ④同素异形体:C60、金刚石、石墨
⑤同位素:1H、2H、3H.
①混合物:冰醋酸、水玻璃、水银 ②化合物:CaCl2、烧碱、聚乙烯
③电解质:明矾、胆矾、硫酸钡 ④同素异形体:C60、金刚石、石墨
⑤同位素:1H、2H、3H.
| A、①③④ | B、③④⑤ |
| C、②③④ | D、②④⑤ |
短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2mol ECln与足量的AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀.下列判断错误的是( )
| A、E是一种非金属元素 |
| B、在ECln中E与Cl之间形成共价键 |
| C、E的一种常见氧化物为EO |
| D、E位于元素周期表的ⅥA族 |
下列表示对应反应的离子方程式正确的是( )
| A、用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+═I2+2H2O | ||||
| B、硝酸银溶液中滴加过量氨水:Ag++NH3?H2O═AgOH↓+NH4+ | ||||
| C、碳酸氢钠的水解:HCO3-+H2O?CO32-+H3O+ | ||||
D、用惰性电极电解氯化镁溶液:2Cl-+2H2O
|
下列关于Fe(OH)3胶体的说法中不正确的是( )
| A、Fe(OH)3胶体与硅酸溶液混合将产生凝聚现象 |
| B、Fe(OH)3胶体粒子在电场影响下将向阳极移动 |
| C、液溶胶中Fe(OH)3胶体粒子不停地做布朗运动 |
| D、光线通过Fe(OH)3胶体时会发生丁达尔现象 |
下列电离方程式中正确的是( )
| A、H2SO4=H2++SO42- |
| B、NaHCO3=Na++H++CO32- |
| C、Ca(OH)2=Ca2++2OH- |
| D、CaCl2=Ca+2+2Cl- |
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )| A、该电池工作时电能转化为化学能 |
| B、该电池中电极a是正极 |
| C、该电池的总反应:2H2+O2═2H2O |
| D、外电路中电子由电极b通过导线流向电极a |
 如图所示的装置,在盛有水的烧杯中,等质量的铁圈和银圈的连接在一起,吊着一根绝缘的细丝,使之平衡.小心地从烧杯中央滴入CuSO4溶液.试回答下列问题:(相对原子质量:Fe-56,Cu-64)
如图所示的装置,在盛有水的烧杯中,等质量的铁圈和银圈的连接在一起,吊着一根绝缘的细丝,使之平衡.小心地从烧杯中央滴入CuSO4溶液.试回答下列问题:(相对原子质量:Fe-56,Cu-64)