题目内容
下列关于Fe(OH)3胶体的说法中不正确的是( )
| A、Fe(OH)3胶体与硅酸溶液混合将产生凝聚现象 |
| B、Fe(OH)3胶体粒子在电场影响下将向阳极移动 |
| C、液溶胶中Fe(OH)3胶体粒子不停地做布朗运动 |
| D、光线通过Fe(OH)3胶体时会发生丁达尔现象 |
考点:胶体的重要性质
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、胶粒遇带相反电荷的胶粒发生聚沉;
B、Fe(OH)3胶粒在电场的作用下,做定向运动,这种现象称为电泳;
C、胶体粒子在不停地做布朗运动;
D、光束通过胶体时,产生光亮的通路,称为丁达尔效应.
B、Fe(OH)3胶粒在电场的作用下,做定向运动,这种现象称为电泳;
C、胶体粒子在不停地做布朗运动;
D、光束通过胶体时,产生光亮的通路,称为丁达尔效应.
解答:
解:A、Fe(OH)3胶体胶粒带正电,硅酸胶体胶粒带负电,二者相遇发生聚沉,故A正确;
B、Fe(OH)3胶粒带有正电荷,所以在电场的作用下,向阴极区移动,而使该区颜色加深,这种现象称为电泳,故B错误;
C、Fe(OH)3胶体粒子不停地做布朗运动,故C正确;
D、光线通过Fe(OH)3胶体时会发生丁达尔现象,故D正确;
故选B.
B、Fe(OH)3胶粒带有正电荷,所以在电场的作用下,向阴极区移动,而使该区颜色加深,这种现象称为电泳,故B错误;
C、Fe(OH)3胶体粒子不停地做布朗运动,故C正确;
D、光线通过Fe(OH)3胶体时会发生丁达尔现象,故D正确;
故选B.
点评:本题考查胶体的性质,难度不大,注意丁达尔效应是胶体的特有性质.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
设NA为阿伏加德罗常数,下列说法中不正确的是( )
| A、2.3g金属钠变为钠离子时失去的电子数是0.1NA |
| B、0.5NA个氯分子所占体积约为11.2L |
| C、28g氮气所含原子数为2NA |
| D、18g水所含的质子总数为10NA |
根据以下实验事实,判断四种微粒在酸性条件下,氧化性由强到弱的顺序是( )
①向FeCl3溶液中滴加KI溶液,再加入CCl4振荡,CCl4层呈紫色;
②向FeCl2溶液中加入氯水,再加入KSCN溶液,呈红色;
③向KMnO4溶液中加入浓盐酸,振荡后紫色褪去.
①向FeCl3溶液中滴加KI溶液,再加入CCl4振荡,CCl4层呈紫色;
②向FeCl2溶液中加入氯水,再加入KSCN溶液,呈红色;
③向KMnO4溶液中加入浓盐酸,振荡后紫色褪去.
| A、I2>Cl2>Fe3+>MnO4- |
| B、MnO4->Cl2>Fe3+>I2 |
| C、Cl2>I2>Fe3+>MnO4- |
| D、Fe3+>MnO4->Cl2>I2 |
下列除杂方案正确的是(括号内为除杂剂)( )
| A、NaOH溶液中混有Ba(OH)2(K2SO4) |
| B、NaCl溶液中混有Na2CO3(盐酸) |
| C、CO中混有CO2(炽热的炭) |
| D、CO2中混有HCl气体(NaOH溶液) |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、若C2H6分子中含共价键数为7NA,则乙烷的体积为22.4L |
| B、58.5g氯化钠固体中含NaCl分子数为NA |
| C、78g液态笨分子中含碳碳双键数目为3NA |
| D、28g N2和6g H2在高温高压铁触媒催化作用下,生成的NH3分子数一定小于2NA |
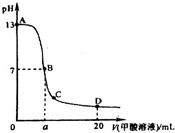 甲酸为一元弱酸,在15mL 0.1mol/L KOH溶液中逐滴加入0.2mol/L甲酸溶液,溶液的pH变化和所加入的甲酸的体积关系描绘成如图所示曲线.下面有关微粒浓度的大小关系正确的是( )
甲酸为一元弱酸,在15mL 0.1mol/L KOH溶液中逐滴加入0.2mol/L甲酸溶液,溶液的pH变化和所加入的甲酸的体积关系描绘成如图所示曲线.下面有关微粒浓度的大小关系正确的是( )| A、在A、B间的任意一点上都存在:c(K+)>c(HCOO-)>c(OH-)>c(H+) |
| B、在B点:c(K+)=c(HCOO-)>c(OH-)=c(H+),且a=7.5 |
| C、在C点:c(HCOO-)>c(K+)>(H+)>c(OH-) |
| D、在D点:c(HCOO-)+c(HCOOH)=2c(K+) |
新型高效多功能水处理剂Na2FeO4的制备方法可用化学方程式表示为:
2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
对此反应下列说法不正确的是( )
2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
对此反应下列说法不正确的是( )
| A、在反应中Na2FeO4只是氧化产物 | ||
B、在反应中有
| ||
| C、2mol FeSO4发生反应时,共有10mol电子转移 | ||
| D、此反应氧化剂为Na2O2 |
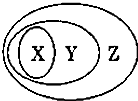 用如图表示的一些物质或概念间的从属关系中,正确的是( )
用如图表示的一些物质或概念间的从属关系中,正确的是( )