题目内容
观察如图几个装置示意图,有关叙述正确的是( )
A、装置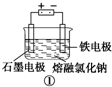 工业上可用于生产金属钠,电解过程中石墨电极产生金属,此法也可用于生产活泼金属镁、铝等 工业上可用于生产金属钠,电解过程中石墨电极产生金属,此法也可用于生产活泼金属镁、铝等 |
B、装置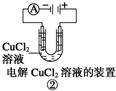 中随着电解的进行左边电极会产生红色的铜,并且电流表示数不断变小 中随着电解的进行左边电极会产生红色的铜,并且电流表示数不断变小 |
C、装置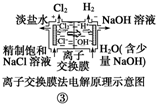 中的离子交换膜只允许阳离子、阴离子和小分子水通过 中的离子交换膜只允许阳离子、阴离子和小分子水通过 |
D、装置 的待镀铁制品应与电源正极相连 的待镀铁制品应与电源正极相连 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.电解池中阴极上金属离子放电生成单质;
B.铜离子在阴极得电子;
C.离子交换膜只允许离子通过;
D.电镀池中,镀层作电解池阳极,待镀金属作阴极.
B.铜离子在阴极得电子;
C.离子交换膜只允许离子通过;
D.电镀池中,镀层作电解池阳极,待镀金属作阴极.
解答:
解:A.装置①中阴极上金属离子放电生成单质,即金属单质在铁电极上生成,故A错误;
B.装置②中铜离子在阴极得电子,则随着电解的进行左边电极会产生红色的铜,并且电流表示数不断变小,故B正确;
C.离子交换膜只允许离子通过,水分子是分子,不能通过,故C错误;
D.装置③中,电镀池中,镀层作电解池阳极,待镀金属作阴极,则待镀铁制品应与电源负极相连,故D错误;
故选B.
B.装置②中铜离子在阴极得电子,则随着电解的进行左边电极会产生红色的铜,并且电流表示数不断变小,故B正确;
C.离子交换膜只允许离子通过,水分子是分子,不能通过,故C错误;
D.装置③中,电镀池中,镀层作电解池阳极,待镀金属作阴极,则待镀铁制品应与电源负极相连,故D错误;
故选B.
点评:本题考查原电池和电解池原理,根据电极上得失电子及离子放电顺序来分析解答,难度中等.

练习册系列答案
相关题目
下列说法或解释不正确的是( )
| A、等物质的量浓度的下列溶液中,①NH4Al(SO4)2②NH4Cl③CH3COONH4④NH3?H2O,c(NH4+)由大到小的顺序是:②>①>④>③ |
| B、室温下,向0.01mol?L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| C、向0.2mol?L-1NaHCO3溶液中加如等体积0.1mol?L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、对于反应N2H4(l)=N2(g)+2H2(g)△H=-50.6kJ?mol-1在任何温度下都能自发进行 |
在如图装置中,a为Fe,b为碳棒,关于此装置的各种叙述正确的是( )


| A、a电极上有气体放出,b电极上无气泡,溶液pH变大 |
| B、a是正极,b是负极 |
| C、导线中有电子流动,外电路中,电子从a极到b极 |
| D、a极上发生了还原反应 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、1mol?L-1的K2SO4溶液中有2NA个K+ |
| B、1mol Cl2与足量铁反应,转移2NA个电子 |
| C、标准状况下,22.4L氨气溶于水,此溶液中含有NA个NH3分子 |
| D、所含溶质为63g的浓硝酸与足量的铜反应,生成的气体分子数为0.5NA |
设NA为阿伏加德罗常数,下列说法中不正确的是( )
| A、2.3g金属钠变为钠离子时失去的电子数是0.1NA |
| B、0.5NA个氯分子所占体积约为11.2L |
| C、28g氮气所含原子数为2NA |
| D、18g水所含的质子总数为10NA |
根据以下实验事实,判断四种微粒在酸性条件下,氧化性由强到弱的顺序是( )
①向FeCl3溶液中滴加KI溶液,再加入CCl4振荡,CCl4层呈紫色;
②向FeCl2溶液中加入氯水,再加入KSCN溶液,呈红色;
③向KMnO4溶液中加入浓盐酸,振荡后紫色褪去.
①向FeCl3溶液中滴加KI溶液,再加入CCl4振荡,CCl4层呈紫色;
②向FeCl2溶液中加入氯水,再加入KSCN溶液,呈红色;
③向KMnO4溶液中加入浓盐酸,振荡后紫色褪去.
| A、I2>Cl2>Fe3+>MnO4- |
| B、MnO4->Cl2>Fe3+>I2 |
| C、Cl2>I2>Fe3+>MnO4- |
| D、Fe3+>MnO4->Cl2>I2 |
新型高效多功能水处理剂Na2FeO4的制备方法可用化学方程式表示为:
2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
对此反应下列说法不正确的是( )
2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
对此反应下列说法不正确的是( )
| A、在反应中Na2FeO4只是氧化产物 | ||
B、在反应中有
| ||
| C、2mol FeSO4发生反应时,共有10mol电子转移 | ||
| D、此反应氧化剂为Na2O2 |
