题目内容
下列表示对应反应的离子方程式正确的是( )
| A、用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+═I2+2H2O | ||||
| B、硝酸银溶液中滴加过量氨水:Ag++NH3?H2O═AgOH↓+NH4+ | ||||
| C、碳酸氢钠的水解:HCO3-+H2O?CO32-+H3O+ | ||||
D、用惰性电极电解氯化镁溶液:2Cl-+2H2O
|
考点:离子方程式的书写
专题:离子反应专题
分析:A.二者反应生成碘和水;
B.二者先生成氢氧化银沉淀,但 随着反应的进行,二者反应生成银氨溶液;
C.碳酸氢根离子水解生成碳酸和氢氧根离子;
D.镁离子和氢氧根离子反应生成氢氧化镁沉淀.
B.二者先生成氢氧化银沉淀,但 随着反应的进行,二者反应生成银氨溶液;
C.碳酸氢根离子水解生成碳酸和氢氧根离子;
D.镁离子和氢氧根离子反应生成氢氧化镁沉淀.
解答:
解:A.二者发生氧化还原反应生成碘和水,离子方程式为2I-+H2O2+2H+═I2+2H2O,故A正确;
B.二者先生成氢氧化银沉淀,但随着反应的进行,二者反应生成银氨溶液,离子方程式为:先发生Ag ++NH3?H2O=AgOH↓+NH4+,后发生:AgOH+2NH3?H2O=[Ag(NH3)2]++OH-+2H2O,故B错误;
C.该方程式为电离方程式,碳酸氢根离子水解生成碳酸和氢氧根离子,其水解方程式为HCO3-+H2O?H2CO3+OH-,故C错误;
D.镁离子和氢氧根离子反应生成氢氧化镁沉淀,方程式为Mg2++2Cl-+2H2O
H2↑+Cl2↑+Mg(OH)2↓,故D错误;
故选A.
B.二者先生成氢氧化银沉淀,但随着反应的进行,二者反应生成银氨溶液,离子方程式为:先发生Ag ++NH3?H2O=AgOH↓+NH4+,后发生:AgOH+2NH3?H2O=[Ag(NH3)2]++OH-+2H2O,故B错误;
C.该方程式为电离方程式,碳酸氢根离子水解生成碳酸和氢氧根离子,其水解方程式为HCO3-+H2O?H2CO3+OH-,故C错误;
D.镁离子和氢氧根离子反应生成氢氧化镁沉淀,方程式为Mg2++2Cl-+2H2O
| ||
故选A.
点评:本题考查了离子方程式正误判断,明确物质的性质及离子方程式的书写规则是解本题关键,注意B中能产生银氨溶液,D中镁离子和生成的氢氧根离子生成沉淀,为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、1mol?L-1的K2SO4溶液中有2NA个K+ |
| B、1mol Cl2与足量铁反应,转移2NA个电子 |
| C、标准状况下,22.4L氨气溶于水,此溶液中含有NA个NH3分子 |
| D、所含溶质为63g的浓硝酸与足量的铜反应,生成的气体分子数为0.5NA |
根据以下实验事实,判断四种微粒在酸性条件下,氧化性由强到弱的顺序是( )
①向FeCl3溶液中滴加KI溶液,再加入CCl4振荡,CCl4层呈紫色;
②向FeCl2溶液中加入氯水,再加入KSCN溶液,呈红色;
③向KMnO4溶液中加入浓盐酸,振荡后紫色褪去.
①向FeCl3溶液中滴加KI溶液,再加入CCl4振荡,CCl4层呈紫色;
②向FeCl2溶液中加入氯水,再加入KSCN溶液,呈红色;
③向KMnO4溶液中加入浓盐酸,振荡后紫色褪去.
| A、I2>Cl2>Fe3+>MnO4- |
| B、MnO4->Cl2>Fe3+>I2 |
| C、Cl2>I2>Fe3+>MnO4- |
| D、Fe3+>MnO4->Cl2>I2 |
关于如图所示装置的叙述,正确的是( )


| A、铜是负极,铜片上有气泡产生 |
| B、铜片质量没有变化 |
| C、电流从锌片经导线流向铜片 |
| D、氢离子在铜片表面被氧化 |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、若C2H6分子中含共价键数为7NA,则乙烷的体积为22.4L |
| B、58.5g氯化钠固体中含NaCl分子数为NA |
| C、78g液态笨分子中含碳碳双键数目为3NA |
| D、28g N2和6g H2在高温高压铁触媒催化作用下,生成的NH3分子数一定小于2NA |
下列反应的离子方程式正确的是( )
| A、氢氧化铜和盐酸反应:OH-+H+═H2O |
| B、钠和水反应:Na+2H2O═Na++2OH-+H2↑ |
| C、铁和足量稀硝酸反应:Fe+2H+═Fe2++H2↑ |
| D、常温下,NaOH溶液和Cl2反应:2OH-+Cl2═Cl-+ClO-+H2O |
将纯锌片和纯铜片按如图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )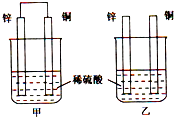

| A、两烧杯中铜片表面均无气泡产生 |
| B、甲中正极的电极反应式为Zn-2e-=Zn2+ |
| C、两烧杯中氢离子浓度均减少 |
| D、产生气泡的速度甲比乙慢 |