题目内容
【题目】黄血盐[亚铁氰化钾K4Fe(CN)6]目前广泛用作食品添加剂(抗结剂),我国卫生部规定实验中黄血盐的最大使用量为10 mg/kg,一种制备黄血盐的工艺如下:
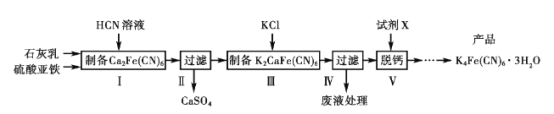
请回答下列问题:
(1)过滤需要用到的玻璃仪器有__________;写出中间产物CaSO4的一种用途__________。
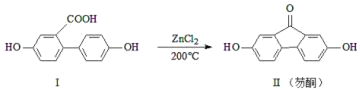
(2)步骤I反应的化学方程式是___________。
(3)步骤V所用的试剂X是________(填化学式),在得到产品前还需经过的步骤包括____。
(4)工艺中用到剧毒的HCN溶液,含CN-等的废水必须处理后才能排放。
①CN-的电子式是_____________。
②处理含CN-废水的方法:第一步NaClO溶液先将CN-不完全氧化为OCN-;第二步NaClO溶液完全氧化OCN-生成N2和两种盐。第二步反应的离子方程式是_____。
(5)已知反应:
3Fe2++2[Fe(CN)6]3- =Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4-=Fe4[Fe(CN)6]3↓(蓝色沉淀)
现有Fe2+被氧化后的溶液,仅供选择的试剂:铁粉、铁氰化钾溶液、亚铁氰化钾溶液、KSCN溶液,请设计检验Fe2+是否氧化完全的实验方案_________。
【答案】漏斗(普通漏斗)、玻璃棒、烧杯 制作石膏或用于制作水泥的原料等(填一种即可) 3Ca(OH)2+ FeSO4+6HCN= Ca2Fe(CN)6+ CaSO4+ 6H2O K2CO3 蒸发浓缩、冷却结晶  3ClO-+ 2OCN-+2OH-= 3Cl-+ 2CO32-+ N2↑+ H2O或3ClO-+ 2OCN-+ H2O = 3Cl-+ 2HCO3-+ N2↑ 取氧化后的溶液少许于试管中,滴加几滴铁氰化钾溶液,若无蓝色沉淀生成,证明Fe2+完全被氧化,否则未完全氧化
3ClO-+ 2OCN-+2OH-= 3Cl-+ 2CO32-+ N2↑+ H2O或3ClO-+ 2OCN-+ H2O = 3Cl-+ 2HCO3-+ N2↑ 取氧化后的溶液少许于试管中,滴加几滴铁氰化钾溶液,若无蓝色沉淀生成,证明Fe2+完全被氧化,否则未完全氧化
【解析】
制备黄血盐的流程步骤一加石灰水、硫酸亚铁、HCN溶液制备Ca2Fe(CN)6,没有化合价变化不属于氧化还原反应,根据步骤二过滤的滤渣CaSO4,确定步骤一的产物中含有CaSO4,故步骤一反应原理为:3Ca(OH)2+ FeSO4+6HCN= Ca2Fe(CN)6+ CaSO4↓+ 6H2O,该过程中CaSO4沉淀生成,步骤二过滤,步骤三加入KCl制备K2CaFe(CN)6:Ca2Fe(CN)6+2KCl= K2CaFe(CN)6↓+ CaCl2,步骤四过滤,滤液进行废水处理,滤渣为K2CaFe(CN)6进行步骤五脱钙处理,在不引入新杂质的原则下,选用K2CO3进行脱钙,过滤得到滤液K4Fe(CN)6,经过蒸发浓缩、冷却结晶、过滤得产品K4Fe(CN)6·3H2O。
(1)过滤需要用到的玻璃仪器有普通漏斗、玻璃棒、烧杯;中间产物CaSO4制作石膏或用于制作水泥的原料等;
(2)根据分析,步骤I反应的化学方程式是3Ca(OH)2+ FeSO4+6HCN= Ca2Fe(CN)6+ CaSO4↓+ 6H2O;
(3)步骤V脱钙过程,一般用碳酸盐脱去钙离子,且不引入新杂质的原则,应该使用碳酸钾,故试剂X为K2CO3;根据分析,步骤五脱钙处理后,对滤液进行蒸发浓缩、冷却结晶、过滤得产品K4Fe(CN)6·3H2O;
(4) ①CN-的电子式是 ;
;
②处理含CN-废水的方法:第一步NaClO溶液先将CN-不完全氧化为OCN-;第二步NaClO溶液完全氧化OCN-生成N2和两种盐,NaClO作氧化剂被还原为NaCl,,每个NaClO化合价降低2。每个OCN中碳元素化合价为+4为最高价不能被氧化,产物以Na2CO3或NaHCO3形式存在,氮的化合价为-3,被氧化为N2,每个氮气分子化合价上升6,故n(ClO):n(N2)=3:1,由于次氯酸钠水解显碱性,则污水处理的第二步对应的离子反应式为:3ClO-+ 2OCN-+2OH-= 3Cl-+ 2CO32-+ N2↑+ H2O或3ClO-+ 2OCN-+ H2O = 3Cl-+ 2HCO3-+ N2↑。
(5) 设计检验Fe2+是否氧化完全的在于检测此时溶液中是否有Fe2+,Fe3+无需检验,则根据已知信息3Fe2++2[Fe(CN)6]3- =Fe3[Fe(CN)6]2↓(蓝色沉淀),实验方案是:取少量氧化后的溶液放于试管中,滴加几滴铁氰化钾溶液,若无蓝色沉淀生成,证明Fe2+完全被氧化,若出现蓝色沉淀,证明还有Fe2+未完全被氧化。

【题目】根据下列实验操作和现象得出的结论正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 将电石与水反应产生的气体通入酸性高锰酸钾溶液 | 溶液紫色褪去 | 证明有乙炔生成 |
B | 取CH3COONa溶液于试管中并加入几滴酚酞,再加热 | 溶液红色加深 | CH3COONa溶液显碱性且存在水解平衡 |
C | 向蔗糖溶液中加入稀硫酸,加热几分钟后加入新制Cu(OH)2悬浊液,加热煮沸 | 无红色沉淀生成 | 蔗糖没有发生水解反应生成葡萄糖 |
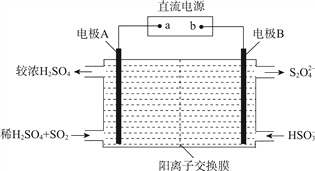
D | 向Na2S2O3溶液中滴加H2SO4溶液至过量 | 一段时间后溶液变浑浊 | Na2S2O3在该反应中只作氧化剂 |
A.AB.BC.CD.D