题目内容
【题目】某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
[查阅资料]
<资料1>该厂采用“侯氏制碱法”生产的化工产品为纯碱(化学式为_____)和氯化铵.(“侯氏制碱法”是我国近代著名科学家侯德榜发明的一种连续生产纯碱与氯化铵的联合制碱工艺.)
<资料2>生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质.
<资料3>部分生产流程如下图所示.
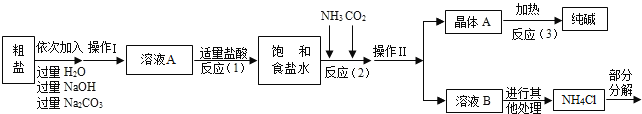
上述流程中涉及的部分反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;Na2CO3+CaCl2=CaCO3↓+2NaCl;NH4Cl═NH3↑+HCl↑
生产原理:将氨气(NH3)和二氧化碳通入饱和食盐水中得到小苏打和氯化铵的混合物,其反应的化学方程式为:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(晶体)↓+NH4Cl;分离出NaHCO3,使其充分受热即可分解制得纯碱及两种常见的氧化物,此反应的化学方程式为_____.
(问题讨论)
(1)溶液A中的溶质为_____,操作Ⅱ的名称为_____.
(2)上述生产流程中可循环使用的是_____(填序号).
ACO2BNH3C.HCl DNaOH ENa2CO3
(3)根据上述信息,请你设计实验区分碳酸钠和碳酸氢钠.
实验步骤 | 实验现象 | 实验结论 |
_____ | _____ | _____ |
(含量测定)
同学们为了测定该纯碱样品的纯度,设计了如下实验.
甲组:取10.0g纯碱样品(假定杂质在整个实验过程中不发生变化),向其中加入过量的盐酸,直至样品中无气泡冒出.充分加热蒸发所得物质并干燥、冷却至室温后称量,所得固体质量为10.9g.样品中碳酸钠的质量分数为_____(结果保留一位小数).
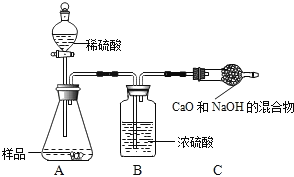
乙组:取10.0g纯碱样品,利用右图所示装置,测出反应后装置C增重了3.5g(所加试剂均足量).
实验结束后,发现乙组测定的质量分数偏小,其原因是_____.
【答案】Na2CO3 2NaHCO3![]() Na2CO3+H2O+CO2↑ NaCl、NaOH、Na2CO3 过滤 ABC 取少量样品中的一种放入试管中,塞上带导管的单孔塞,导管的另一端伸入澄清的石灰水中;加热固体并观察现象. 产生无色气泡,澄清的石灰水变浑浊 该样品是碳酸氢钠;另一种是碳酸钠 86.7% 生成的二氧化碳气体没有被C中的碱石灰完全吸收
Na2CO3+H2O+CO2↑ NaCl、NaOH、Na2CO3 过滤 ABC 取少量样品中的一种放入试管中,塞上带导管的单孔塞,导管的另一端伸入澄清的石灰水中;加热固体并观察现象. 产生无色气泡,澄清的石灰水变浑浊 该样品是碳酸氢钠;另一种是碳酸钠 86.7% 生成的二氧化碳气体没有被C中的碱石灰完全吸收
【解析】
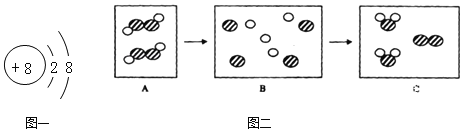
[查阅资料]<资料1>纯碱是碳酸钠的俗名,它由钠离子和碳酸根离子构成,钠的化合价为+1,碳酸根的化合价为﹣2,根据化合物中元素化合价的代数和为0,以及正价在前,负价在后的原则,化学式为Na2CO3;
<资料3>根据信息“分离出NaHCO3,使其充分受热即可分解制得纯碱及两种常见的氧化物”知,反应物为碳酸氢钠,条件是加热,生成物除碳酸钠外,还有两种常见的氧化物,根据碳酸氢钠的组成判断应是水和二氧化碳,故方程式为2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
[问题讨论]
(1)粗盐中含有少量可溶性杂质(MgCl2和CaCl2),氯化镁能与氢氧化钠反应生成氢氧化镁沉淀和氯化钠;氯化钙能与碳酸钠反应生成碳酸钙沉淀和氯化钠,所以A中的溶质主要是氯化钠,由于氢氧化钠和碳酸钠过量,溶液A中也有氢氧化钠和碳酸钠;过滤是把固体与液体分开的操作,操作Ⅱ将混合物分成了晶体与溶液,正是通过过滤操作;
(2)根据生产流程中涉及的方程式和流程图,发现二氧化碳、氨气、氯化氢为重复使用的物质;
(3)碳酸钠化学性质稳定,碳酸氢钠受热易分解生成碳酸钠、水、二氧化碳,而二氧化碳能使澄清的石灰水变浑浊,据此可设计实验:将固体放在试管中加热,并将试管口塞上装有导管的单孔塞,将导管末端伸入澄清石灰水中,石灰水变浑浊,固体为碳酸氢钠,反之,为碳酸钠;
[含量测定]
甲组:
解:设样品中碳酸钠的质量为x.
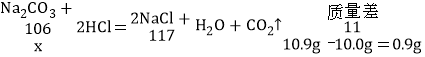
![]() x=8.67g
x=8.67g
样品中碳酸钠的质量分数为![]() ×100%=86.7%
×100%=86.7%
乙组:乙组测定的质量分数偏小,其直接原因是C装置增重少,可能原因是生成的二氧化碳气体没有被C中的碱石灰完全吸收。

【题目】金属资源在生活中有着极其广泛的应用。
(1)铝的广泛存在及应用
①铝在地壳中的含量居所有金属元素第_____位。
②铝是很活泼的金属,但用铝制作的炊具却耐腐蚀,其原因是_____(以方程式表示)。 长期使用铝制炊具会使人体摄入过量的“铝”,不利人体健康。这里的“铝”是指_____。
a单质 b元素 c原子 d分子
③明矾中也含有铝元素,生活中用明矾净水的原理是_____。
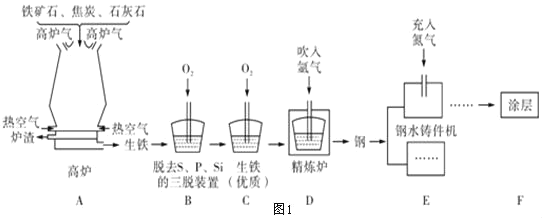
(2)铁的冶炼:图1为某钢铁公司的矿石选取、冶铁和炼钢的工艺流程。
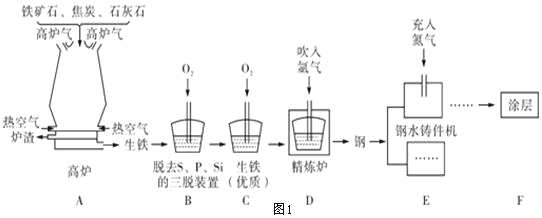
①用赤铁矿石冶铁的反应原理是_____(用化学方程式表示)。
②分析工艺流程,三脱装置中发生反应的化学方程式是_____(任写一个)。
③在钢水铸件机中,高温钢加工成钢制零件时,充入氮气的作用是_____。
(3)铁的防护:某同学为探究铁制品锈蚀的条件,进行如下实验:
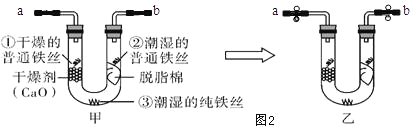
步骤 1:利用图甲所示装置,将干燥的O2从导管
a 通入U形管(装置气密性良好,药品如图甲所示);待U形管内充满O2,用止水夹夹紧导 管a、b 处连接胶皮管,如图乙所示。
步骤 2:一段时间后,观察U形管内的铁丝,其现象如表所示。
实验序号及对象 | 现象 |
①干燥的普通铁丝 | 没有明显变化 |
②潮湿的普通铁丝 | 较多红褐色锈斑 |
③潮湿的纯铁丝 | 没有明显变化 |
①步骤1中,如何证明U形管内O2已充满?_____。
②水是铁制品锈蚀的条件之一,此实验中_____(填实验序号)作对比能证明该结论。
③通过此实验还可得出影响铁制品锈蚀的因素是_____。
【题目】金属资源在生活中有着极其广泛的应用。
(1)铝的广泛存在及应用
①铝在地壳中的含量居所有金属元素第_____位。
②铝是很活泼的金属,但用铝制作的炊具却耐腐蚀,其原因是_____(以方程式表示)。 长期使用铝制炊具会使人体摄入过量的“铝”,不利人体健康。这里的“铝”是指_____。
a单质 b元素 c原子 d分子
③明矾中也含有铝元素,生活中用明矾净水的原理是_____。
(2)铁的冶炼:图1为某钢铁公司的矿石选取、冶铁和炼钢的工艺流程。
①用赤铁矿石冶铁的反应原理是_____(用化学方程式表示)。
②分析工艺流程,三脱装置中发生反应的化学方程式是_____(任写一个)。
③在钢水铸件机中,高温钢加工成钢制零件时,充入氮气的作用是_____。
(3)铁的防护:某同学为探究铁制品锈蚀的条件,进行如下实验:
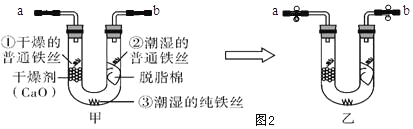
步骤 1:利用图甲所示装置,将干燥的O2从导管
a 通入U形管(装置气密性良好,药品如图甲所示);待U形管内充满O2,用止水夹夹紧导 管a、b 处连接胶皮管,如图乙所示。
步骤 2:一段时间后,观察U形管内的铁丝,其现象如表所示。
实验序号及对象 | 现象 |
①干燥的普通铁丝 | 没有明显变化 |
②潮湿的普通铁丝 | 较多红褐色锈斑 |
③潮湿的纯铁丝 | 没有明显变化 |
①步骤1中,如何证明U形管内O2已充满?_____。
②水是铁制品锈蚀的条件之一,此实验中_____(填实验序号)作对比能证明该结论。
③通过此实验还可得出影响铁制品锈蚀的因素是_____。
【题目】下列知识整理的内容不完全正确的一组是( )
A化学反应基本类型 | B化学与生活 |
①化合反应C+O2 ②解反应H2CO3=H2O+CO2↑ ③置换反应C+2CuO ④复分解反应HCl+AgNO3=AgCl↓+HNO3 | ①液氧﹣﹣可用于火箭的助燃剂 ②人体缺乏碘元素﹣导致甲状腺肿大 ③鉴别羊毛和合成纤维﹣点燃后闻气味 ④用洗洁精除去餐具油污一利用乳化作用 |
C化学实验数据记录 | D化学中常见的“三” |
①托盘天平称取7.8g铁粉 ②250mL量筒量取47.25mL水 ③用pH试纸测得苹果汁的pH为3.2 | ①煤、石油、天然气一一三大化石燃料 ②塑料、合成纤维、合成橡胶﹣﹣三大合成材料 ③分子、原子、离子一一构成物质的三种基本粒子 |
A. AB. BC. CD. D