题目内容
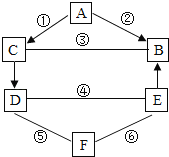
【题目】A,B,C,D,E,F都是初中化学常见的物质,它们之间的关系如下图所示.(图中“﹣”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系.)其中:B是常用于光合作用和灭火的气体,D是一种微溶于水的物质,且D的溶解度随温度的升高而减小.反应①②③的基本反应类型相同;反应④⑤⑥中,一个有沉淀生成,另一个有气体生成,还有一个没有明显现象.B与E不含相同元素,D与F只含一种相同元素.
(1)A的化学式为_____,E的化学式为_____.
(2)反应①的化学方程式为_____,基本反应类型为_____.
(3)反应⑥的化学方程式为_____.
【答案】O2 HCl O2+2H2![]() 2H2O 化合反应 Na2CO3+2HCl=2NaCl+CO2↑+H2O
2H2O 化合反应 Na2CO3+2HCl=2NaCl+CO2↑+H2O
【解析】
B可以用于光合作用和灭火,B就一定是二氧化碳,D微溶于水,且溶解度随温度的升高而减小,D就是氢氧化钙,A会转化成二氧化碳和C,反应①②③的基本反应类型相同, C就是水,A就是氧气,①②③均发生化合反应;反应④⑤⑥中,一个有沉淀生成,另一个有气体生成,还有一个没有明显现象,氢氧化钙哦盐酸反应生成水和氯化钙,反应无明显现象,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和水,碳酸钠和盐酸反应生成二氧化碳气体,B与E不含相同元素,故E为氯化氢(盐酸),D与F只含一种相同元素,F为碳酸钠;
(1)根据分析可知,A为氧气,E为氯化氢;
(2)氢气和氧气在点燃的条件下生成水,O2+2H2![]() 2H2O,反应是由两种物质生成一种物质,符合“多变一”,为化合反应;
2H2O,反应是由两种物质生成一种物质,符合“多变一”,为化合反应;
(3)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,反应方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O。

 名校课堂系列答案
名校课堂系列答案【题目】牙膏是一种日用必需品。某研究性学习小组对某一品牌牙膏中所含摩擦剂的成分进行了如下探究。
[查阅资料]
(1)牙膏常用氢氧化铝、碳酸钙、二氧化硅等物质作摩擦剂,牙膏中其它成分遇到盐酸时无气体生成;SiO2不溶于水也不与盐酸反应。
(2)氢氧化铝是两性氢氧化物,在常温下它既能与强酸,又能与强碱反应。如与氢氧化钠可发生如下反应:Al(OH)3+NaOH=NaAlO2+2H2O.(NaAlO2溶于水)
[提出问题]该品牌牙膏的酸碱性如何?其中含有什么摩擦剂?
[实验与猜想]
(1)取少量牙膏膏体于小烧杯中,加入10毫升蒸馏水,充分搅拌,静置一段时间,分离上层清液和沉淀,待用;
(2)用pH试纸测定所得溶液的pH大于7,正确的操作方法是_____。
(3)取少量沉淀物加入过量的稀盐酸,沉淀物全部溶解并有大量气泡产生,同时得到澄清溶液A,则该品牌牙膏中一定含有碳酸钙,一定不含有_____。
(4)进行猜想:摩擦剂成分可能是a。只含碳酸钙 b._____。
[设计实验]
实验步骤 | 实验现象 | 解释与结论 |
取澄清溶液A逐滴滴入一定量氢氧化钠溶液 | 开始无明显现象,后产生白色沉淀 | 原因是1._____,2._____。(用化学方程式表示) |
继续滴入氢氧化钠溶液直至过量 | _____ | 摩擦剂中还含有_____ |
[实验结论]该品牌牙膏所含摩擦剂的成分猜想b正确。
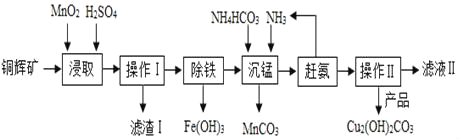
【题目】某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
[查阅资料]
<资料1>该厂采用“侯氏制碱法”生产的化工产品为纯碱(化学式为_____)和氯化铵.(“侯氏制碱法”是我国近代著名科学家侯德榜发明的一种连续生产纯碱与氯化铵的联合制碱工艺.)
<资料2>生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质.
<资料3>部分生产流程如下图所示.
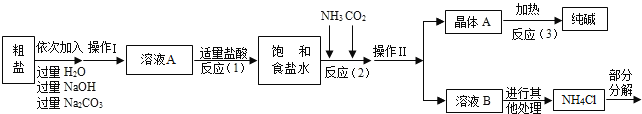
上述流程中涉及的部分反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;Na2CO3+CaCl2=CaCO3↓+2NaCl;NH4Cl═NH3↑+HCl↑
生产原理:将氨气(NH3)和二氧化碳通入饱和食盐水中得到小苏打和氯化铵的混合物,其反应的化学方程式为:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(晶体)↓+NH4Cl;分离出NaHCO3,使其充分受热即可分解制得纯碱及两种常见的氧化物,此反应的化学方程式为_____.
(问题讨论)
(1)溶液A中的溶质为_____,操作Ⅱ的名称为_____.
(2)上述生产流程中可循环使用的是_____(填序号).
ACO2BNH3C.HCl DNaOH ENa2CO3
(3)根据上述信息,请你设计实验区分碳酸钠和碳酸氢钠.
实验步骤 | 实验现象 | 实验结论 |
_____ | _____ | _____ |
(含量测定)
同学们为了测定该纯碱样品的纯度,设计了如下实验.
甲组:取10.0g纯碱样品(假定杂质在整个实验过程中不发生变化),向其中加入过量的盐酸,直至样品中无气泡冒出.充分加热蒸发所得物质并干燥、冷却至室温后称量,所得固体质量为10.9g.样品中碳酸钠的质量分数为_____(结果保留一位小数).
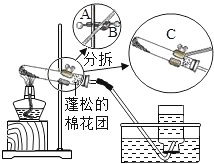
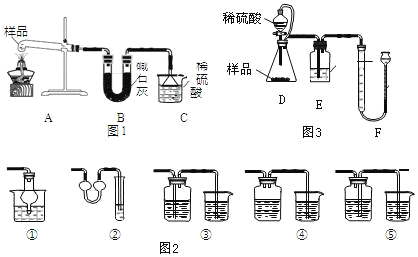
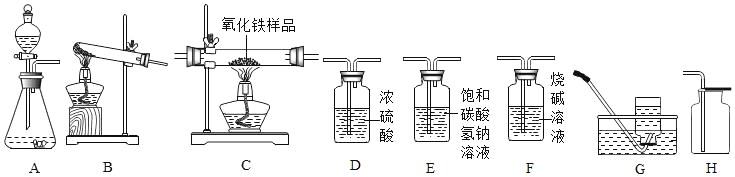
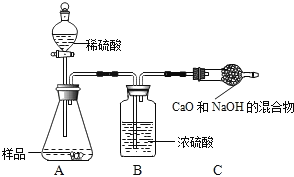
乙组:取10.0g纯碱样品,利用右图所示装置,测出反应后装置C增重了3.5g(所加试剂均足量).
实验结束后,发现乙组测定的质量分数偏小,其原因是_____.