题目内容
【题目】某实验小组对过氧化氢分解反应进行探究:
(探究一)探究影响过氧化氢分解快慢的因素。实验步骤及现象如下:
分别取5mLH2O2溶液进行实验,测定产生4mLO2所需时间,实验结果记录如下:
实验序号 | H2O2溶液的浓度 | 温度℃ | MnO2粉末用量/g | 反应时间 |
① | 30 | 35 | 0 | t1 |
② | 30 | 55 | 0 | t2 |
③ | 5 | 20 | 0.1 | t3 |
④ | 15 | 20 | 0.1 | t4 |
(1)对比①②两个实验,若t1>t2,则可得出的结论是:_____。
(2)能说明过氧化氢分解快慢与其浓度有关的实验是_____(填实验序号)。
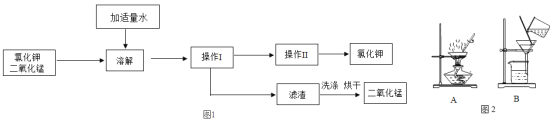
(探究二)探究氧化铁(Fe2O3)能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?实验步骤及现象如下:
实验步骤 | 实验现象 |
Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入0.5g氧化铁粉末,并将带火星的木条分别伸入A、B两支试管中,观察现象。 | A试管中产生大量气泡,带火星的木条复燃;_____ |
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把火星的木条伸入试管中,观察现象。 | 试管中产生大量气泡,带火星的木条复燃; |
Ⅲ.待实验Ⅱ中没有现象时,将试管中的反应剩余物过滤,并将滤渣洗涤、干燥、称量。 | 所得固体质量为_____g; |
Ⅳ.分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入0.5g氧化铁粉末,向D试管中加入0.5g二氧化锰粉末,观察现象。 | —— |
(1)补充完成上述实验探究中表格的实验现象:①_____。②_____g。
(2)继续完成以下问题:
(实验结论)
①实验II、III证明_____。综上所述:氧化铁可以作过氧化氢分解的催化剂。
②写出氧化铁催化过氧化氢分解的符号表达式_____。
(实验评价)
③实验设计IV的目的是_____;
(实验拓展)
④查阅资料得知,氧化铜、硫酸铜、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是_____。
A 二氧化锰只能作过氧化氢溶液分解的催化剂
B 同一个化学反应可以有多种催化剂
C 催化剂只能加快化学反应的速率
D 用作催化剂的物质也可能是其他反应的反应物或生成物
【答案】温度会影响过氧化氢溶液的分解,温度越高,分解速率越快 ③④ B试管中产生少量气泡,带火星的木条没有复燃 0.5 氧化铁在反应前后质量和化学性质没有改变 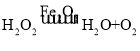 比较氧化铁和二氧化锰对过氧化氢溶液分解的催化效果 BD
比较氧化铁和二氧化锰对过氧化氢溶液分解的催化效果 BD
【解析】
探究一:
(1)对比①②两个实验,若t1>t2,则可得出的结论是温度会影响过氧化氢溶液的分解,温度越高,分解速率越快。
(2)③④实验过氧化氢浓度不一样,其他条件一样,故能说明过氧化氢分解快慢与其浓度有关的实验是③④。
探究二:
(1)Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入0.5g氧化铁粉末,B中未加入催化剂,故A试管中产生大量气泡,带火星的木条复燃,B试管中产生少量气泡,带火星的木条没有复燃。
Ⅲ.待实验Ⅱ中没有现象时,将试管中的反应剩余物过滤,并将滤渣洗涤、干燥、称量,催化剂在反应前后质量不变,所得固体质量为0.5g.
(2)实验结论:
①Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管中,试管中产生大量气泡,带火星的木条复燃,说明氧化铁的化学性质未改变,Ⅲ中氧化铁质量未改变,故实验II、III证明氧化铁在反应前后质量和化学性质没有改变,综上所述:氧化铁可以作过氧化氢分解的催化剂。
②氧化铁催化过氧化氢分解生成水和氧气,反应的符号表达式为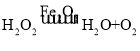 。
。
实验评价:
③实验设计IV的目的是比较氧化铁和二氧化锰对过氧化氢溶液分解的催化效果;
实验拓展:
④A 二氧化锰不只能作过氧化氢溶液分解的催化剂,还可以做氯酸钾分解的催化剂,说法错误;
B 同一个化学反应可以有多种催化剂,说法正确;
C 催化剂能加快化学反应的速率,也能减慢化学反应的速率,说法错误;
D 用作催化剂的物质也可能是其他反应的反应物或生成物,如二氧化锰可以是催化剂,也是高锰酸钾分解的产物,说法正确。
故填:BD。

 阅读快车系列答案
阅读快车系列答案【题目】古人云“处处留心皆学问”,你若善于观察,就会获取更多的新知识。
(发现问题)在一次探究活动中,小强用塑料吸管向新制的澄清石灰水中吹气,在吹气的过程中发现石灰水先出现浑浊,后又变澄清,他感到很意外。于是小强又将纯净的二氧化碳通入新制的澄清石灰水中,观察到的现象与上次相同。
(1)请写出石灰水变浑浊的方程式________;小强做第二个实验的目的是________________。
(2)小强从老师那里得知:CO2能与CaCO3和H2O继续反应生成Ca(HCO3)2。由此,小强推测出Ca(HCO3)2的一条物理性质是能溶于水,写出CO2与CaCO3和H2O反应生成Ca(HCO3)2的化学方程式_________________________。
此外,小强还想了解Ca(HCO3)2的化学性质,提出了如下猜想:
(提出猜想)Ca(HCO3)2受热能否分解?
(查阅资料)Ca(HCO3)2受热分解生成CaCO3、H2O和CO2
(设计方案)小强用高锰酸钾制取氧气的发生装置来加热Ca(HCO3)2,加热时试管口要略_________倾斜,目的是__________________________________________。
(实验过程)小强在实验室找到一瓶Ca(HCO3)2粉末,取少量放入试管中进行加热,观察到试管口附近有小液滴产生。据此,小强得出结论:Ca(HCO3)2受热能够分解。
(反思评价)(1)小波认为小强的实验不能证明Ca(HCO3)2受热一定分解了,小波的理由是_______。
(2)请你设计实验方案,验证加热过程中有CO2产生。
选用试剂 | 实验操作方法 | 预想实验现象 | 结论 |
澄清石灰水 | 取适量Ca(HCO3)2粉末于试管中进行加热,将产生气体通入澄清石灰水中 | _________________ | 有CO2生成 |
(3)小红发现 CO2与CaCO3和H2O反应生成Ca(HCO3)2的化学反应方程式与Ca(HCO3)2受热分解的方程式在形式上近乎相反,于是联想到二氧化碳溶于水的过程也有类似情况,进行了如下课后小实验:
①将二氧化碳气体通入紫色石蕊溶液中,观察现象;
②将第①步实验得到的溶液置于酒精的火焰上加热,观察现象。
则下列选项中与小红进行的①②两步实验中石蕊溶液颜色变化情况相符是____(填字母)
A 紫色→红色→无色 B 红色→紫色→无色
C 红色→紫色→红色 D 紫色→红色→紫色
写出小红第①步实验中发生的反应的化学方程式_________________________,小红第②步实验中发生的化学反应属于__________反应(填反应类型)。
【题目】根据表中内容回答下列问题。
| 0 | 20 | 40 | 60 | 80 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
Ca(OH)2 | 0.173 | 0.165 | 0.121 | 0.116 | 0.094 |
(1)将接近饱和的澄清石灰水变为饱和,除增加溶质的方法以外,还可以通过___、____达到。
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是____。
(3)向20℃的氢氧化钙饱和溶液中加入少量生石灰,再冷却至20℃,此时溶液中溶质的质量比加入生石灰前溶液中溶质的质量____(填“增大”、“不变”或“减小”)。
(4)20℃时,氯化钠饱和溶液中溶质的质量分数为____(结果保留至0.1%)。
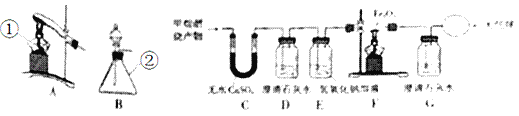
【题目】某兴趣小组对KClO3分解反应的催化剂进行探究,在相同的加热条件下,用如图装置完成表中实验:
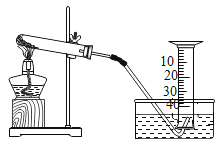
编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50 mLO2所需时间/s |
实验1 | 5 | ﹣ | ﹣ | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
(1)设置实验1的目的是______________。
(2)表中所列3种催化剂的催化效果最佳的是______________(填物质名称),该物质为_____________色固体。写出KClO3在该物质催化下受热分解的符号表达式:__________________。
(3)KClO3中Cl元素的化合价为_______________,试写出KClO3中的阴离子_____________。
(4)由实验1和实验4可知,KCl__________(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集50 mL O2,所需时间明显少于171 s,解释原因:______________。
(5)要比较KClO3分解反应中不同催化剂的催化效果,除了测量收集50 mL O2所需时间外,还可以测量相同时间内_____________。
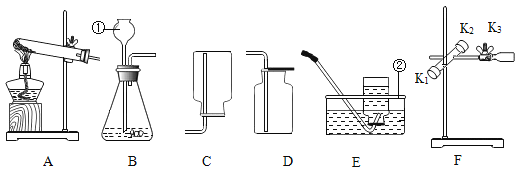
【题目】下图是实验室常用的制取气体的发生装置和收集装置。
(1)实验室用A装置制取氧气的化学方程式是______________,实验室用B装置制取氧气的化学方程式是________________。
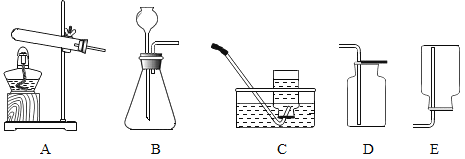
(2)实验室常用块状固体硫化亚铁(FeS)和稀硫酸在常温下制取硫化氢气体,有关化学方程式为:![]() ,硫化氢气体是一种有臭鸡蛋气味的有毒的气体,能溶于水,根据上述信息回答:实验室制取硫化氢的发生装置为___________(用字母序号填空),收集装置为___________(用字母序号填空)。
,硫化氢气体是一种有臭鸡蛋气味的有毒的气体,能溶于水,根据上述信息回答:实验室制取硫化氢的发生装置为___________(用字母序号填空),收集装置为___________(用字母序号填空)。
(3)某实验小组的同学用碳酸钠粉末、粒状大理石、稀盐酸、浓盐酸、稀硫酸这几种药品,探究哪两种药品的反应适合在实验室制取CO2。请你参与下列的探究并回答问题。
(提出问题)上述酸和碳酸盐的反应是否适合在实验室制取CO2?
(方案设计)大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO2,你认为原因是_________________。
讨论后大家设计了如下三个实验进行对比分析。
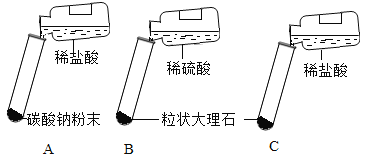
(实验与结论)
实验 | 实验现象 | 实验内容 |
A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
B | 产生气泡,速率迅速减慢,反应几乎停止。 | 无法持续产生CO2,不能用于实验室制取CO2 |
C | 产生气泡,速率适中 | 速率适中持续产生CO2,能用于实验室制取CO2 |
根据探究结论,实验室制取二氧化碳选择第C组药品,该药品制取二氧化碳的反应原理为___________________________ (用化学方程式表示)_______________;验满方法是______________; 检验方法二氧化碳的是__________________。
(拓展与迁移)
(4)由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等。请你再写出一种需要考虑的因素:________________________。
(5)如图:为了探究二氧化碳能否与水反应,现取用三朵紫色石蕊染成的干花(石蕊是一种色素,它遇酸变成红色)进行实验。
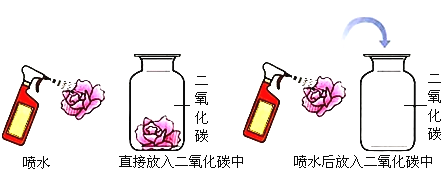
现象:第一朵紫色干花喷上水,紫花不变色 ;第二朵紫色干花直接放入盛满二氧化碳的集气瓶中,紫花也不变色;第三朵紫色干花先喷上水,再放入盛二氧化碳的集气瓶中,紫花_______(填写关于颜色的现象)。
结论:以上实验现象说明: ________________。反应的化学方程式是:___________________________________