题目内容
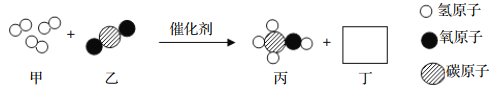
【题目】2017年5月,我国在南海海域成功开采可燃冰。可燃冰外观像冰,主要成份是甲烷水合物(甲烷分子和水分子组成),可表示为 CH4nH2O,在开采过程中,若甲烷泄漏会导致严重的温室效应。
某化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,设计实验探究:
(提出问题)甲烷燃烧后生成哪些物质?
(查阅资料)①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;
②白色无水CuSO4粉末遇水变蓝色;
③CO与人体内的血红蛋白结合,会造成人中毒缺氧。
(猜想与假设)猜想一:CO2、H2O; 猜想二:CO、H2O;猜想三:CO2、CO、H2O
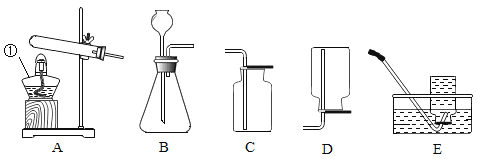
(实验探究)将甲烷在一定量的纯净氧气中燃烧的产物依次通过C﹣G装置(部分夹持、固定装置省略)进行验证:
(1)装置A、B中标有数字的仪器名称 ①_____,②_____。
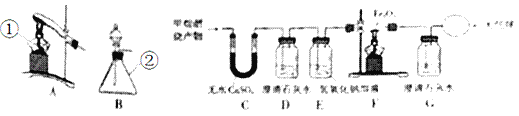
若选用过氧化氢溶液和二氧化锰来制取氧气,应选用的发生装置是_____;该反应的化学方程式为_____;
(2)实验过程中观察到C中白色粉末变为蓝色,D、G中澄清石灰水变浑浊,F中红色粉末变成黑色,由此推断猜想_____成立。
(3)实验过程中D装置的作用是_____;该反应的化学方程式是_____。
(4)实验过程中用纯净O2而不用空气的原因是_____。
(5)实验过程中C、D装置的顺序不能颠倒,原因是_____。
(反思与交流)日常生活中,使用含碳燃料一定要注意通风,防止_____中毒。
【答案】 酒精灯 锥形瓶 B 2H2O2![]() 2H2O+O2↑ 三 检验二氧化碳 Ca(OH)2+CO2═CaCO3↓+H2O 空气中含有水蒸气和二氧化碳,影响检验结果 气体通过澄清石灰水时会带出水蒸气 一氧化碳
2H2O+O2↑ 三 检验二氧化碳 Ca(OH)2+CO2═CaCO3↓+H2O 空气中含有水蒸气和二氧化碳,影响检验结果 气体通过澄清石灰水时会带出水蒸气 一氧化碳
【解析】本题考查了实验探究物质的组成成分,常见气体的检验与除杂方法,化学方程式的书写等。解答时要根据各种物质的性质,结合各方面条件进行分析、判断得出正确的结论。
实验探究:(1)①是酒精灯,②是锥形瓶;
若选用过氧化氢溶液和二氧化锰来制取氧气,反应不需要加热,应选用的发生装置是B,过氧化氢与二氧化锰混合生成水和氧气,反应的化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)实验过程中观察到C中白色粉末变为蓝色,说明反应生成了水,D、G中澄清石灰水变浑浊,F中红色粉末变成黑色,说明反应生成了一氧化碳和二氧化碳,由此推断猜想三成立。
(3)实验过程中D装置的作用是检验二氧化碳,这是因为二氧化碳能和氢氧化钙反应生成碳酸钙沉淀和水,该反应的化学方程式是:Ca(OH)2+CO2═CaCO3↓+H2O;
(4)实验过程中用纯净O2而不用空气的原因是空气中含有水蒸气和二氧化碳,影响检验结果;
(5)实验过程中C、D装置的顺序不能颠倒,原因是气体通过澄清石灰水时会带出水蒸气,影响对水蒸气的检验。
反思与交流:日常生活中,使用含碳燃料一定要注意通风,防止一氧化碳中毒。