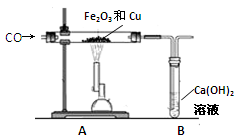
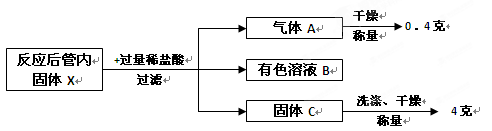
题目内容
某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如图所示,请回答: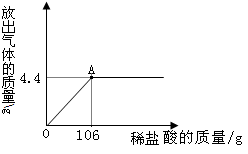
(1)当加入212g稀盐酸时,放出气体的质量为__________g
(2)碳酸钠样品中碳酸钠的质量分数为多少?(写出计算过程)
(3)加入106g稀盐酸(即A点)时烧杯中溶液溶质的质量分数为多少?(写出计算过程)
(1)4.4g(2)80%(3)10%
解析试题分析:(1)根据图像,可以看出当加入106g稀盐酸的时候,反应就结束,产生气体质量为4.4g,所以当加入212g稀盐酸时,放出气体的质量仍然为4.4g
(2)发生反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑,根据方程式中碳酸钠与二氧化碳的质量关系可算出碳酸钠的质量,进而可以计算碳酸钠样品中碳酸钠的质量分数,反应后得到的是NaCl溶液,所以也可根据方程式中NaCl与二氧化碳的质量关系,求出溶液中溶质的质量
解:设碳酸钠的质量为x,生成的NaCl质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
100:44=x:4.4g x=10.6g
(2)碳酸钠样品中碳酸钠的质量分数=10.6g/13.25g×100%=80%
117:44=y:4.4g y=11.7g 又由于反应后溶液质量=10.6g+95.8g+106g-4.4g=208g
(3)溶液溶质的质量分数=11.7g/208g×100%=5.6%
考点:根据化学方程式进行的计算

 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案(6分)为测定Cu一Zn合金的组成,小华同学利用该合金粉末与稀硫酸反应,进行了三次实验,所得相关实验数据记录如下:
| | 第一次 | 第二次 | 第三次 |
| 所取合金的质量/g | 1O | 10 | 20 |
| 加入硫酸的质量/g | 50 | 80 | 50 |
| 生成氢气的质量/g | 0.2 | 0.2 | 0.2 |
(1)从上表数据分析,当所取合金与所用稀硫酸的质量比为 时,表明合金中的锌与稀硫酸恰好完全反应;
(2)该合金中锌的质量为多少克?(计算结果保留一位小数)
(3)所用合金中的锌与稀硫酸恰好完全反应时所得溶液中溶质的质量分数为多少?(计算结果精确到0.1%)
长期使用的水壶底部结有一层水垢,其主要成分是碳酸钙和氢氧化镁,为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用如图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表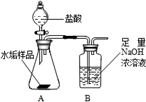
| | 第一次 | 第二次 | 第三次 | 平均值 |
| B装置增加的质量 | 2.17 | 2.22 | 2.21 | |
(1)第一次实验测得数据较低的原因是___________;
(2)平均每份水垢样品中碳酸钙的质量为___________克.
下图是某药厂生产补钙剂的商品标签图。
| XXX儿童咀嚼片(60片装) |
| [主要成分]:碳酸钙、维生素 [功效]:补钙 [规格]:2.5g/片、每片中含:碳酸钙≥25%、维生素D:100IU [食用方法]:嚼食、每日一片 |
请你根据以上标标签信息完成下列计算
(1)主要成分碳酸钙的相对分子质量为 ;每片药剂中至少含钙元素的质量为 克。
(2)小红同学为测定其碳酸钙的含量标注是否属实。她取出4片研碎后放入烧杯中,逐滴加入稀盐酸至不再放出气体为止。共用去稀盐酸40g。称量烧杯中剩余物的质量为47.8g(不含烧杯质量,假定钙片其他成分不与盐酸反应。)求:
① 生成二氧化碳的质量
② 通过计算判断每片钙片中碳酸钙的含量是否属实[CaCO3+2HCl=CaCl2+H2O+CO2↑]
长时间使用的热水壶底部有一层水垢,主要成分是CaCO3。某校化学研究性学习小组同学通过实验想测定水垢中CaCO3的含量。他们取100g水垢,加入足量的稀盐酸,同时测量5分钟(min)内生成CO2质量,测量数据如下表:
| 时间/ min | 1 | 2 | 3 | 4 | 5 |
| 生成CO2的质量/g | 15 | 25 | 30 | 33 | 33 |
②请根据表格分析写出你发现的一条规律是 。
③该水垢中CaCO3的质量分数是多少?
 Na2SO4+2NH3↑+2H2O,
Na2SO4+2NH3↑+2H2O,