��Ŀ����
����Ŀ��С�ƃ�ѧ�Ķ��������ϵ�֪��ijЩ������ɴ������������һЩ��Ӧ�Ĵ������������Դ˲�����̽����Ȥ��
���ᳫ���⣩����ͭ�ܷ�������طֽ�Ĵ�����
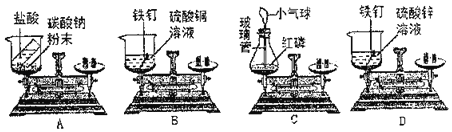
�����ʵ�飩С���������������ʵ�飨��������Ӱ��ʵ������ؾ����ԣ�
ʵ���� | KC1O3/g | ������ | ��������������mL�� | ��ʱ��s�� |
1 | 0.6 | / | 9.8 | 480 |
2 | 0.6 | 0.2g����ͭ | 67 | 90 |
3 | 0.6 | 0.2g�������� | 67 | 37 |
��1��д��������ö��������������Ļ�ѧ����ʽ______��
��2����ʵ��1��ʵ��2�����ݿ�֪������ͭ______��ѡ��ܡ����ܡ����ӿ�����صķֽ����ʡ�
��3��Ϊ֤������ͭ�Ǹ÷�Ӧ�Ĵ�����С������������µ�ʵ�顣
1����ʵ��2��Ӧ��Ļ�����������ˮ�ܽ⣬���ˣ�ϴ�Ӳ�ʮ�����ƽ����������Ϊ0.2g��
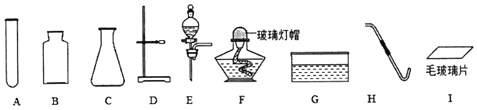
��������COͨ���˳��Ĺ��壬����ͼ����ʵ�飬С��ͬѧ��ʵ�鱨�����±�������д�ո��е����ݡ�
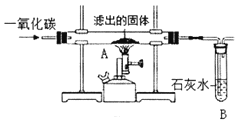
װ�� | ���� | ���� |
A | ______ | ������ͭ |
B | �����ʯ��ˮ��ɻ��� | �����˶�����̼ |
���ó����ۣ�ͨ��I����ʵ��֤������ͭ��������طֽ�Ĵ�����
����˼�����ۣ�
�ӻ����Ƕȷ�������ͼװ���в���֮��������Ϊ����θĽ���______��
���𰸡�2KClO3![]() 2KCl+3O2�� �� ��ɫ��ĩ��� ȼ�ŵľƾ��ƶ�β�����д���
2KCl+3O2�� �� ��ɫ��ĩ��� ȼ�ŵľƾ��ƶ�β�����д���
��������
��1������غͶ������̼��������Ȼ��غ���������Ӧ��ѧ����ʽ2KClO3![]() 2KCl+3O2����
2KCl+3O2����
��2������ʵ�������֪����ͭ�ܼӿ�����صķֽ����ʣ�
��3��һ����̼������ͭ��Ӧ����ͭ�Ͷ�����̼����������Ϊ��ɫ��ĩ��죻
[��˼������]һ����̼�ж�����Ҫ����β������������B���һ�����һ��һյȼ�ŵľƾ��ơ�