题目内容
【题目】空气是自然界赋予人类的重要资源。研究空气的成分,正确认识空气,合理利用空气是化学的任务之一。
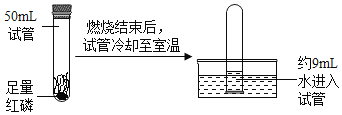
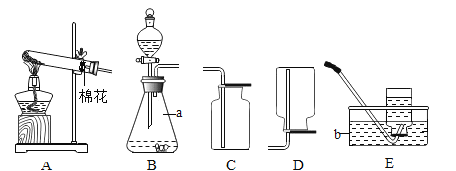
(1)某同学利用燃磷法测定空气中氧气含量,实验过程如图所示。
①该实验测得氧气的体积分数约是______%.与实际值进行对比,说明存在误差的可能原因是______。
②燃烧结束时,试管里剩余气体的主要性质是______。
【答案】18 装置漏气 不能燃烧,不能支持燃,难溶于水
【解析】
(1)
①试管的体积为50mL,约9mL水进入试管,则该实验测得氧气的体积分数约是9mL÷50mL=18%,故填18;红磷足量,温度冷却至室温,与实际值进行对比,结果仍偏小,存在误差的可能原因是装置漏气(在冷却过程中有外界的空气进入瓶中),故填装置漏气;
②足量的红磷燃烧一段时间后熄灭,说明剩余的主要气体氮气不能燃烧,不能支持燃烧,进入的水的体积为9mL,水不再继续进入,说明氮气难溶于水,故填不能燃烧,不能支持燃,难溶于水。

【题目】小科冋学阅读课外资料得知,某些氧化物可代替二氧化锰作一些反应的催化剂,于是她对此产生了探究兴趣、
(提倡问题)氧化铜能否作氯酸钾分解的催化剂?
(设计实验)小科设计了下列三组实验(其他可能影响实验的因素均忽略)
实验编号 | KC1O3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
1 | 0.6 | / | 9.8 | 480 |
2 | 0.6 | 0.2g氧化铜 | 67 | 90 |
3 | 0.6 | 0.2g二氧化锰 | 67 | 37 |
(1)写出氯酸钾用二氧化锰作催化剂的化学方程式______。
(2)从实验1与实验2的数据可知,氧化铜______(选填“能”或“不能”)加快氯酸钾的分解速率。
(3)为证明氧化铜是该反应的催化剂,小科又完成了以下的实验。
1,将实验2反应后的混合物加足量的水溶解,过滤,洗涤并十燥,用天平称量,质量为0.2g。
Ⅱ.将过量的CO通入滤出的固体,按如图进行实验,小科同学的实验报告如下表,请填写空格中的内容。
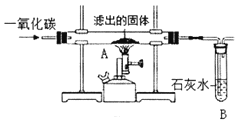
装置 | 现象 | 结论 |
A | ______ | 生成了铜 |
B | 澄清的石灰水变成浑浊 | 产生了二氧化碳 |
(得出结论)通过I、Ⅱ实验证明氧化铜能作氯酸钾分解的催化剂。
(反思与评价)
从环保角度分析,上图装置有不足之处,你认为该如何改进?______。