1. 能量判据(ΔH<0):多数自发进行的化学反应是放热反应
2. 熵判据(ΔS>0):熵增有利于自发,同一物质熵值:S(固) S(液) S(气)
3. 复合判据(△G = △H - T△S 0)
[思考]请填写下列表格(用自发反应,非自发反应,不一定)
|
|
ΔS >0 |
ΔS <0 |
|
ΔH >0 |
|
|
|
ΔH <0 |
|
|
[例1]下列变化过程中,ΔS<0的是( )
A.氯化钠溶于水中 B.NH3和HCl反应生成NH4Cl(固)
C.干冰的升华 D.碳酸钙分解为CaO和C02
[例2]以下自发反应可用能量判据来解释的是( )
A.硝酸铵自发地溶于水; B.2N2O5(g) = 4NO2(g)+ O2(g) △H=+56.7kJ/mol;
C.(NH4 )2CO3(s)=NH4HCO3(s)+NH3(g) △H=+74.9 kJ/mol; D.2H2(g)+ O2(g)=2H2O(l) △H=-571.6 kJ/mol。
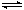 [例6])将1.00molSO2(g)和1.00molO2(g)放入容积为1L的密闭容器中,在1000K达到平衡:2SO2(g) + O2(g) 2SO3(g),测得c(SO3)=0.925mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
[例6])将1.00molSO2(g)和1.00molO2(g)放入容积为1L的密闭容器中,在1000K达到平衡:2SO2(g) + O2(g) 2SO3(g),测得c(SO3)=0.925mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。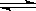 2HI(g),△H<0
2HI(g),△H<0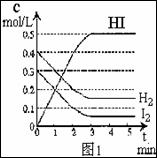
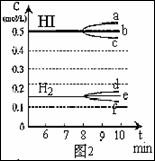
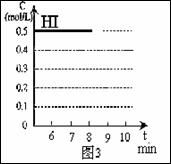
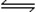 1.表达式:aA +bB c cC+dD K=
1.表达式:aA +bB c cC+dD K=
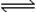 [例4]下列方法中可以证明2HI H2
+ I2(g)已达到平衡状态的是
[例4]下列方法中可以证明2HI H2
+ I2(g)已达到平衡状态的是 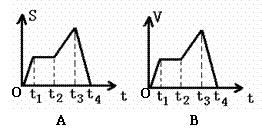 在今年的“运动图像”习题课上,我设计如图所示的两个曲线图形,希望通过分析讲解,帮助学生区别 “匀变速直线运动的速度--时间图像和位移--时间图像”的物理意义。然而在讲完本题后,并没有达到期望的效果,仍然有一部分同学表示不能理解。我本想用准备好的多媒体课件展示它们的区别,此时有一位同学示意他可以用走动的方法表示它们的区别,我请他说出方法,他走到讲台中间,向同学们介绍他的做法,接着他先按图A的图像走动(边走边讲解):向教室门口方向走去(0-t1时段),停了几秒钟(t1-t2时段),又向门口走去(t2-t3时段),再接着又转身走回开始的位置(t3-t4时段);又按图B的图像走动:先加速小跑几步(0-t1时段),接着匀速走几步(t1-t2时段),又加速跑几步(t2-t3时段),然后还是向前越来越慢的走几步(t3-t4时段),直至停下。他的这种表示方法,同学们用热烈的掌声表示赞赏,好多同学产生了浓厚的兴趣,纷纷举手要求上台走动。我深受启发,立即改变原来的设计,同意让几个同学上台表演,大部分同学都能正确表示,也有几个在t3-t4时段出现错误,经过下面同学大声的指正,最后都表示能理解这两个图像的区别。由于本节课学生独特的表示方法,引起了其他同学极大的兴趣,课堂气氛相当活跃,学生不仅理解了两种图像的物理意义,大大增强了他们的参与热情,效果比多做几道习题好得多。
在今年的“运动图像”习题课上,我设计如图所示的两个曲线图形,希望通过分析讲解,帮助学生区别 “匀变速直线运动的速度--时间图像和位移--时间图像”的物理意义。然而在讲完本题后,并没有达到期望的效果,仍然有一部分同学表示不能理解。我本想用准备好的多媒体课件展示它们的区别,此时有一位同学示意他可以用走动的方法表示它们的区别,我请他说出方法,他走到讲台中间,向同学们介绍他的做法,接着他先按图A的图像走动(边走边讲解):向教室门口方向走去(0-t1时段),停了几秒钟(t1-t2时段),又向门口走去(t2-t3时段),再接着又转身走回开始的位置(t3-t4时段);又按图B的图像走动:先加速小跑几步(0-t1时段),接着匀速走几步(t1-t2时段),又加速跑几步(t2-t3时段),然后还是向前越来越慢的走几步(t3-t4时段),直至停下。他的这种表示方法,同学们用热烈的掌声表示赞赏,好多同学产生了浓厚的兴趣,纷纷举手要求上台走动。我深受启发,立即改变原来的设计,同意让几个同学上台表演,大部分同学都能正确表示,也有几个在t3-t4时段出现错误,经过下面同学大声的指正,最后都表示能理解这两个图像的区别。由于本节课学生独特的表示方法,引起了其他同学极大的兴趣,课堂气氛相当活跃,学生不仅理解了两种图像的物理意义,大大增强了他们的参与热情,效果比多做几道习题好得多。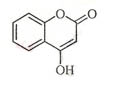 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成: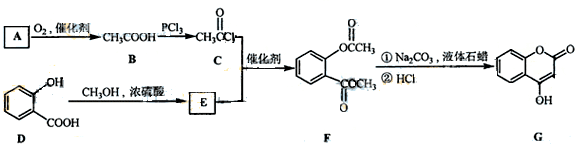
 (3)
(3)

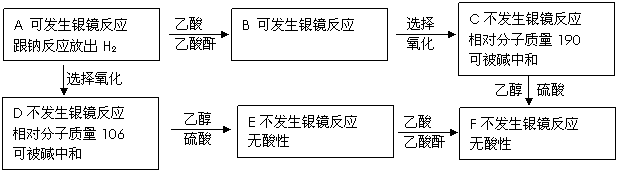
 [解析](1)A与银氨溶液反应有银镜生成,则A中存在醛基,由流程可知,A与氧气反应可以生成乙酸,则A为CH3CHO;
[解析](1)A与银氨溶液反应有银镜生成,则A中存在醛基,由流程可知,A与氧气反应可以生成乙酸,则A为CH3CHO;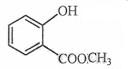 ;
;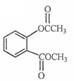 +3NaOH→
+3NaOH→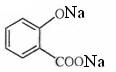 +CH3COONa+CH3OH+H2O;
+CH3COONa+CH3OH+H2O;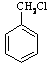 和其他无机物合成
和其他无机物合成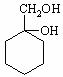 最合理的方案(不超过4步),请在答题纸的方框中表示。
最合理的方案(不超过4步),请在答题纸的方框中表示。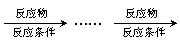 例:
例: [解析]分析目标产物的结构可知,相邻碳上各引入一个羟基要引入碳碳双键。而
[解析]分析目标产物的结构可知,相邻碳上各引入一个羟基要引入碳碳双键。而