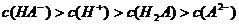17.(12分)有关元素X、Y、Z、W的信息如下:
|
元素 |
信息 |
|
X |
所在主族序数与所在周期序数之差为4 |
|
Y |
最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
|
Z |
单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
|
W |
基态原子核外5个能级上有电子,且最后的能级上只有1个电子 |
请回答下列问题:
(1)W的单质与Y的最高价氧化物对应的水化物反应的离子方程式为
(2)铜片、碳棒和ZX3溶液组成原电池,写出正极发生的电极反应方程式
(3)向淀粉碘化钾溶液中滴加几滴ZX3的浓溶液,现象为 ,Z3+离子的电子排布式为 ,它有 个未成对电子。
(4)以上述所得WX3溶液为原料制取无水WX3,先制得WX3·6H2O晶体,主要操作包括 ,在 条件下加热WX3·6H2O晶体,能进一步制取无水WX3,其原因是(结合离子方程式简要说明) 。
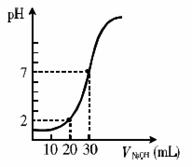
14.右图为室温下20 mL一定物质的量浓度的盐酸,用一定物质的量浓度的NaOH溶液滴定的图示,据图推出盐酸和NaOH溶液的物质的量浓度(mol·L-1)分别是 ( )
|
|
A |
B |
C |
D |
|
c(HCl)(mol·L-1) |
0.06 |
0.04 |
0.03 |
0.09 |
|
c(NaOH)(mol·L-1) |
0.04 |
0.06 |
0.09 |
0.03 |
9.下述实验不能达到预期目的的是 ( )
|
编号 |
实验内容 |
实验目的 |
|
A |
将SO2通入酸性KMnO4溶液中 |
证明SO2具有漂白性 |
|
B |
将Cl2通入NaBr溶液中,然后加入CCl4,振荡、静置 |
比较氯与溴的氧化性强弱 |
|
C |
将铜片分别与浓、稀硝酸反应 |
探究浓、稀硝酸氧化性的相对强弱 |
|
D |
向盛有20g蔗糖的烧杯中加入几滴水,搅拌均匀。再加入少许浓硫酸,迅速搅拌。 |
探究浓硫酸的脱水性 |
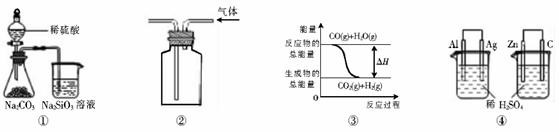
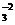 +2H+====CO2↑+H2O
+2H+====CO2↑+H2O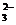 )+
)+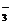 )
)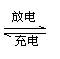
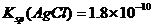 ,则在0.1mol·L-1AlCl3溶液中,Ag+的物质
,则在0.1mol·L-1AlCl3溶液中,Ag+的物质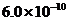 mol·L-1
mol·L-1