物质的检验是化学实验中的重要内容,也是高考的常考内容,通常包括物质的鉴定、鉴别和推断。试题可以是选择题,也有的融于推断、实验、简答题之中。这部分内容是以离子的检验、气体的制备和检验、元素化合物性质为知识基础,以化学实验基本操作,对材料的组织水平和语言表达能力为基础进行考查,且考查的内容逐渐加深,形式渐趋多样化。
物质的分离与提纯从高考的内容和形式来看,主要特点有三个:一是选取适当的试剂及其分离的方法除去被提纯物中指定的杂质;二是确定除去被提纯物中指定含有的杂质和所需加入试剂的先后顺序:三是将分离、提纯与物质制备、混合物成分的确定等内容融为一体,形成综合实验题。解答混合物分离提纯内容的试题一般应先弄清实验目的,再分析所依据的实验原理,由此去选择适宜的试剂、分离的方法,并回答相关的问题。
物质的分离、提纯操作及应注意的问题,判断操作的正确与错误,根据要求选择实验仪器;分离、提纯、鉴别物质时选择适当的试剂是高考的重点考查内容。其中,不用任何化学试剂区别一组(通常是四种)物质的实验是高考经常考查的热点。
[例1]有甲酸、乙酸、乙醛、乙酸乙酯、乙醇、溴乙烷6种无色溶液,只用一种试剂便可将它们一一鉴别开来。这种试剂是
A.蒸馏水 B.FeCl3溶液
C.Cu(OH)2浊液 D.NaOH溶液
解析:Cu(OH)2会与甲酸、乙酸发生中和反应,生成易溶的羧酸铜溶液。甲酸和乙醛有醛基,加热时会被Cu(OH)2氧化,Cu(OH)2还原出砖红色的Cu2O沉淀。Cu(OH)2悬浊液中有水,当与酯或溴乙烷相混时,有机层与水层因不溶而分离,酯密度小,浮于水面,溴乙烷密度大,沉于下层。
答案:C
[例2]某硝酸钠固体中混有少量硫酸铵和碳酸氢钠杂质,试设计一实验方案,即除去杂质,又配成硝酸钠溶液。供选用的试剂有:①稀HCl、②稀HNO3、③稀H2SO4、④NaOH溶液、⑤Na2CO3溶液、⑥BaCl2溶液、⑦Ba(OH)2溶液、⑧Ba(NO3)2溶液,供选用的实验操作有
A.加热 B.过滤 C.分液
D.蒸发 E.蒸馏 F.结晶
实验方案:先将固体溶于蒸馏水配成溶液,然后填表完成各步实验(只填试剂或操作的序号,要求试剂不超过3种,空格按要求填写,可不填满)。
|
选择试剂 |
|
|
|
|
|
实验操作 |
|
|
|
|
解析:依题意,本题实际上要除去NH 、SO
、SO 、HCO
、HCO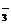 ,从选用试剂尽可能少考虑,可选用过量Ba(OH)2,加入Na2CO3除去过量的Ba2+,再加入HNO3以除去过量的CO
,从选用试剂尽可能少考虑,可选用过量Ba(OH)2,加入Na2CO3除去过量的Ba2+,再加入HNO3以除去过量的CO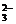 和OH-,故选择试剂⑦、⑤、②,实验操作A、B、A。
和OH-,故选择试剂⑦、⑤、②,实验操作A、B、A。
答案:⑦ ⑤ ② A B A
1.物质的检验
(1)鉴定、鉴别与推断的比较
|
|
不同点 |
相同点 |
|
鉴定 |
根据物质的化学性质,对一种物质分别检验出阴、阳离子 |
均需根据物质的特征反应,选择恰当的试剂和方法,准确观察反应中颜色变化、沉淀的生成或溶解、气体的生成、焰色等现象加以判定 |
|
鉴别 |
对两种或两种以上的物质进行辨认 |
|
|
推断 |
通过已知实验事实,根据性质分析,推出被检物质的组成或名称 |
(2)常见物质的检验方法
根据物质性质(主要是化学性质,物理性质往往也是重要线索),使被检验物质与加入的试剂作用,转变为某种已知物质,或产生某种特殊现象,从而确定该物质的存在。常见的特殊现象有:
①生成气体:能够生成气体的离子很多,生成的气体也常有性质的相似之处,判断时要注意干扰。
②生成沉淀:许多金属阳离子或酸根阴离子都可生成具有特殊颜色、特殊性质的沉淀,但同时也应注意排除干扰离子。
③显现特殊颜色:特殊颜色的出现或消失并配合特殊试剂,是鉴别物质的常见方法,如KSCN检验Fe3+、苯酚检验Fe3+、酸性KMnO4检验不饱和化合物、新制Cu(OH)2悬浊液检验醛类物质等。



