20.(10分)已知稀溴水和氯化铁溶液都呈黄色,某化学活动小组进行实验探究。
李强、王刚两同学分别在足量的稀氯化亚铁溶液中,加入1-2滴液溴,振荡后溶液呈黄色。
(1)李强同学认为这不是发生化学反应所致,则使溶液呈黄色的微粒是: ▲ (填粒子的化学式);王刚同学则认为这是发生化学反应所致,试写出对应的离子方程式: ▲ 。
(2)如果要验证王刚同学判断的正确性,请根据下面所提供的可用试剂,用两种方法加以验证,请将选用的试剂代号及实验中观察到的现象填入下表。
实验可供选用试剂: A.碘化钾淀粉溶液 B.氢氧化钠溶液 C.硝酸银溶液
D.硫氰化钾溶液 E.四氯化碳 F.酸性高锰酸钾溶液
|
实验方案 |
所选用试剂(填代号) |
实验现象 |
|
方案一 |
▲ |
▲ |
|
方案二 |
▲ |
▲ |
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入少量氯气,则首先被氧化的离子是
▲ (填粒子的化学式);若在稀溴化亚铁溶液中通入过量氯气,则相应的离子方程式为 ▲ 。
15.(10分)
资料1.据《重庆晚报》2009.8.12报道:在全民补碘政策实施15年之后的今天,来自民间和医学界自主补碘的呼声越来越高。加碘食盐是“防病”还是“致病”?甲状腺疾病频发是否与碘营养过量有关?中国食盐加碘“一刀切”政策或将面临深层次的调整。
资料2.下表是某食用碘盐包装袋上的部分说明:
|
配 料 |
食盐、碘酸钾、抗结剂 |
|
碘含量 |
35±15mg/kg |
|
储藏方法 |
密封、避光、防潮 |
|
食用方法 |
烹饪时,待食品熟后加入碘盐 |
请回答下列问题:
(1)下列说法正确的是 ▲ 。
A.碘酸钾易挥发 B.高温会导致碘的损失
C.用淀粉就能直接检验碘盐中的碘酸钾 D.碘酸钾可氧化氯化钠
(2)碘酸钾与碘化钾在酸性条件下发生如下反应:KIO3+KI+H2SO4→K2SO4+I2+H2O(未配平)该化学方程式配平后系数依次为 ▲ 。该反应的还原剂为 ▲ ;1mol KIO3完全反应转移的电子总数为 ▲ 。
(3)碘不能多也不能少。已知:I2+2S2O32-=2I-+S4O62-,我校化学兴趣小组测定某食用碘盐中碘的含量。其步骤为:
①准确称取w g食盐,加适量蒸馏水使其完全溶解;②用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;③以淀粉为指示剂,逐滴加入物质的量浓度为1.0×10-3mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。则所测盐中碘的含量是(以含w的代数式表示) ▲ mg/kg。
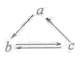
14.下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
|
|
a |
b |
c |
|
A |
Al |
AlCl3 |
 Al(OH)3 Al(OH)3 |
|
B |
NO |
NO2 |
HNO3 |
|
C |
Si |
SiO2 |
H2SiO3 |
|
D |
H2SO4 |
SO2 |
SO3 |
第Ⅱ卷(非选择题 共72分)
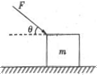 D.加速度方向不变而速度方向变化
D.加速度方向不变而速度方向变化 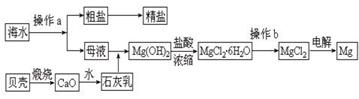
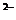 恰好沉淀完全:
恰好沉淀完全: 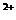 =BaSO4↓
=BaSO4↓