用电解法制取KIO3的方法是以石墨和铁为电极电解KI溶液,电解反应方程式为
KI + 3H2O KIO3 + 3H2↑。下列说法中正确的是
KIO3 + 3H2↑。下列说法中正确的是
| A.电解时石墨作阴极 |
| B.电解时阳极上产生H2 |
| C.电解过程中阴极区溶液pH升高 |
| D.阴极电极反应式:I-- 6e-+ 3H2O = IO3-+ 6H+ |
镀锌钢管具有广泛的用途,镀锌钢管有冷镀锌管和热镀锌管,冷镀即电镀,热镀是指熔融状态的锌与铁生成合金层。下列说法正确的是
| A.铁锌形成的合金层是纯净物,耐酸碱腐蚀 |
| B.钢管镀锌的目的是使铁与锌形成原电池,消耗锌而保护钢管免受腐蚀 |
| C.钢管冷镀时,钢管作阴极,锌棒作阳极,锌盐溶液作电解质溶液 |
| D.镀锌钢管破损后,负极反应式为Fe-2e-=Fe2+ |
铅蓄电池是典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42一 2PbSO4+2H2O。下列说法正确的是
2PbSO4+2H2O。下列说法正确的是
| A.放电时,负极的电极反应式是PbO2+4H++SO42一+2e一=PbSO4+2H2O |
| B.充电时,电解液中H2SO4的浓度将变小 |
| C.放电时,PbO2发生氧化反应 |
| D.充电时,蓄电池的正极和外接电源的正极相连 |
某小组设计如图装置(盐桥中盛有浸泡了KNO3溶液的琼脂)研究电化学原理。下列叙述正确的是( )
| A.银片为负极,发生的反应为:Ag++e-= Ag |
| B.进行实验时,琼脂中K+移向Mg(NO3)2溶液 |
| C.用稀硫酸代替AgNO3溶液,可形成原电池 |
| D.取出盐桥,电流表依然有偏转 |
液体燃料电池相比于气体燃料电池具有体积小等优点。一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是( )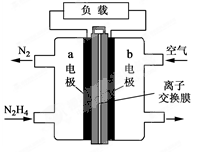
| A.b极发生氧化反应 |
| B.a极的反应式:N2H4+4OH--4e-=N2↑+4H2O |
| C.放电时,电流从a极经过负载流向b极 |
| D.其中的离子交换膜需选用阳离子交换膜 |
一种碳纳米管能够吸附氢气,可做充电电池(如右图所示)的碳电极,该电池的电解质为6 mol/L KOH溶液,下列说法中正确的是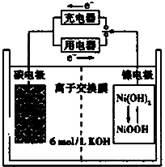
| A.充电时将碳电极与电源的正极相连 |
| B.充电时阴极发生氧化反应 |
| C.放电时镍电极反应为:NiO(OH)+H2O+e-=Ni(OH)2+OH- |
| D.放电时碳电极反应为:2H++2e—=H2 ↑ |
下图所示装置I是一种可充电电池,装置Ⅱ为电解池。离子交换膜只允许Na+通过,充放电的化学方程式为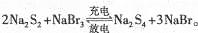 闭合开关K时,b极附近先变红色。下列说法正确的是
闭合开关K时,b极附近先变红色。下列说法正确的是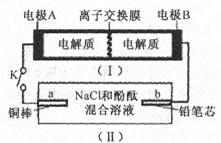
| A.当有0.01 mol Na+通过离子交换膜时,b电极上析出112 mL的气体 |
| B.负极反应为3Br--2e-= Br3- |
| C.闭合K后,b电极附近的pH变小 |
| D.闭合K后.a电极上有氯气产生 |
阿波罗宇宙飞船上使用的是氢氧燃料电池,其电极总反应式为2H2+O2=2H2O;电解质溶液为KOH溶液,反应保持在较高温度,使水蒸发,下列叙述正确的是
| A.此电池能见到浅蓝色火焰 |
| B.H2为正极,O2为负极 |
| C.工作时电解液的OH-的物质的量不断增加 |
| D.电极反应为负极H2失电子;正极O2得电子 |
在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是
| A.正极附近SO42-浓度逐渐增大 |
| B.电子通过导线由铜片流向锌片 |
| C.正极反应式为Zn-2e-=Zn2+ |
| D.该原电池工作过程中电解质溶液的pH增大 |
