题目内容
液体燃料电池相比于气体燃料电池具有体积小等优点。一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是( )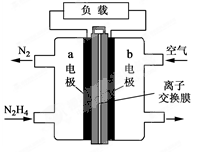
| A.b极发生氧化反应 |
| B.a极的反应式:N2H4+4OH--4e-=N2↑+4H2O |
| C.放电时,电流从a极经过负载流向b极 |
| D.其中的离子交换膜需选用阳离子交换膜 |
B
解析试题分析:通入燃料N2H4的电极a作负极,通入氧气的电极b作正极。负极发生反应N2H4+4OH--4e-=N2↑+4H2O;正极发生反应:O2+4e-+2H2O=4OH-.放电时电子从a极经过负载流向b极。电流则电流从b极经过负载流向a极. 由于在反应过程中不断消耗OH-或生成OH-离子。因此其中的离子交换膜需选用阴离子交换膜。根据上述分析可知正确选项为B.
考点:考查燃料电池的工作原理的知识。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
利用如图装置,完成很多电化学实验。下列有关此装置的叙述中,正确的是( )
| A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阴极保护法 |
| B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阴离子向铁电极移动 |
| C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动 |
| D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小 |
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图。下列有关氢氧燃料电池的说法不正确的是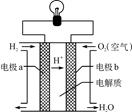
| A.该电池工作时化学能转化为电能 |
| B.该电池中电极b是正极,发生还原反应 |
| C.外电路中电流由电极a通过导线流向电极b |
| D.该电池的总反应:2H2+O2=2H2O |
a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块如图所示放置一段时间。下列有关描述错误的是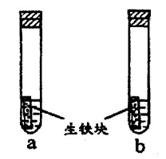
| A.生铁块中的碳是原电池的正极 |
| B.a试管内压强变大,b试管内压强变小 |
C.两试管中相同的电极反应式是:2Fe Fe2++2e- Fe2++2e- |
| D.两试管中均发生了电化腐蚀 |
查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为X,其中一个电极的反应式为CH3CH2OH-2e-=X+2H+。下列说法中正确的是 ( )
| A.电池内部H+由正极向负极移动 |
| B.另一极的电极反应式为:O2+4e-+2H2O=4OH- |
| C.乙醇在正极发生反应,电子经过外电路流向负极 |
| D.电池总反应为:2CH3CH2OH+O2=2CH3CHO+2H2O |
在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是
| A.正极附近SO42-浓度逐渐增大 |
| B.电子通过导线由铜片流向锌片 |
| C.正极反应式为Zn-2e-=Zn2+ |
| D.该原电池工作过程中电解质溶液的pH增大 |
如图为氢氧燃料电池示意图,按此图的提示,下列叙述不正确的是( )。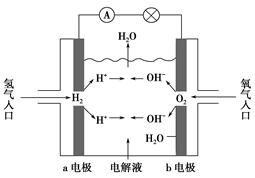
| A.a电极是负极 |
| B.b电极的电极反应为:4OH--4e-=2H2O+O2↑ |
| C.氢氧燃料电池是一种具有应用前景的绿色电源 |
| D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
目前,科学家提出了一种经济而且理想的获得氢能源的循环体系(如图)。关于此循环体系,下列说法中错误的是( )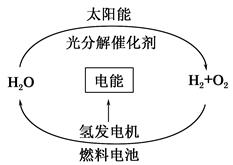
| A.燃料电池能够使化学反应产生的能量转化为电能 |
| B.燃料电池中通入H2的一极作负极,发生氧化反应 |
| C.在此循环中发生了反应:2H2O??2H2↑+O2↑ |
| D.目前化学家急需解决的问题是寻找合适的光照条件下分解水的催化剂 |
燃料电池能有效提高能源利用率,具有广泛的应用前景。下列物质均可用作燃料电池的燃料,其中最环保的是( )
| A.甲醇 | B.天然气 | C.液化石油气 | D.氢气 |