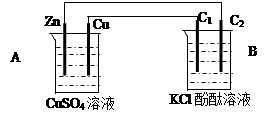我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4Al + 3O2 + 6H2O = 4Al(OH)3,下列说法不正确的是( )
| A.正极反应式为:O2 + 2H2O + 4e- = 4OH- |
| B.电池工作时,电流由铝电极沿导线流向铂电极 |
| C.以网状的铂为正极,可增大与氧气的接触面积 |
| D.该电池通常只需更换铝板就可继续使用 |
用质量均为100g的铜作电极,电解硝酸银溶液(足量),电解一段时间后,两电极的质量差为28g,此时两电极的质量分别为( )
| A.阳极100g,阴极128g | B.阳极93.6g,阴极121.6g |
| C.阳极91.0g,阴极119.0g | D.阳极86.0g,阴极114.0g |
将锌片和铜片按图示方式插入柠檬中,电流计指针发生偏转。下列针对该装置的说法正确的是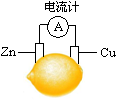
| A.将电能转化为化学能 |
| B.电子由铜片流出 |
| C.锌片是负极. |
| D.铜片逐渐被腐蚀 |
某课外活动小组用如图所示装置进行实验(电解液足量)。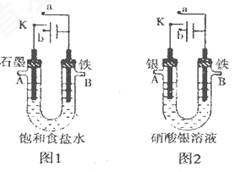
下列说法中错误的是
A.圈l中,若开始实验时开关K与a连接,则B极的电极反应式为 |
| B.图l中,若开始实验时开关K与b连接,则一段时间后向电解液中通入适量HCl气体可恢复到电解前的浓 |
| C.图2中,若开始实验时开关K与a连接,则电解液的溶质质量分数变小 |
| D.图2中,若开始实验时开关K与b连接,则A极减少 |
下列叙述正确的是
| A.在电解池的阴极和原电池的负极上都发生氧化反应 |
| B.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
| C.用惰性电极电解KOH溶液,阴、阳两极产物的物质的量之比为1:2 |
| D.用惰性电极电解饱和NaCl溶液,若有lmol电子转移,则生成l molNaOH |
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上并压紧(如下图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大。)
依据记录数据判断,下列结论中正确的是
| A.将甲、乙形成的合金露置在空气中,甲先被腐蚀 |
| B.金属乙能从硫酸铜溶液中置换出铜 |
| C.在四种金属中丙的还原性最弱 |
| D.甲、丁若形成原电池时,甲为正极 |
某研究性学习小组进行电化学实验,研究装置如图所示。
有关说法不正确的是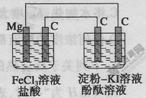
| A.镁为负极 |
| B.原电池中碳极的电极反应式为Fe3++e-=Fe2+ |
| C.电解池中阳极处先变红 |
| D.电解池中阴极的电极反应式为2H++2e-=H2↑ |
银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液中,一段时间后发现黑色会褪去。下列说法正确的是
| A.处理过程中银器一直保持恒重 |
| B.银器为正极,Ag2S被还原生成单质银 |
| C.该过程中总反应为2Al+3Ag2S═6Ag+Al2S3 |
| D.黑色褪去的原因是黑色Ag2S转化为白色AgCl |
用惰性电极电解一定浓度的硫酸铜溶液,长时间通电后,向所得溶液中加入0.2mol Cu(OH)2,恰好恢复到电解前的浓度和pH。则电解过程中转移电子的总物质的量为
| A.0.2mol | B.0.4mol | C.0.6mol | D.0.8mol |