题目内容
某研究性学习小组进行电化学实验,研究装置如图所示。
有关说法不正确的是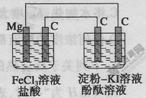
| A.镁为负极 |
| B.原电池中碳极的电极反应式为Fe3++e-=Fe2+ |
| C.电解池中阳极处先变红 |
| D.电解池中阴极的电极反应式为2H++2e-=H2↑ |
C
解析试题分析:据图可知,左池为原电池,镁活泼作负极,C为正极,电极反应为Fe3++e-=Fe2+;右池为电解池,与Mg相连的电极为阴极,电极反应式为2H++2e-=H2↑,与C相连的电极为阳极,电极反应为:2I--2e-=I2,故可使淀粉变蓝。故C错误。
考点:考查电化学的相关知识。

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
观察下列几个装置示意图,有关叙述正确的是
| A.装置①中阳极上析出红色固体 |
| B.装置②的待镀铁制品应与电源负极相连 |
| C.装置③中外电路电子由b极流向a极 |
| D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |
如下图是工业电解饱和食盐水的装置示意图,下列有关说法中不正确的是
| A.装置中出口①处的物质是氯气,出口②处的物质是氢气 |
| B.装置中发生反应的离子方程式为:2Cl-+2H+通电Cl2↑+H2↑ |
| C.该装置是将电能转化为化学能 |
| D.该离子交换膜只能让阳离子通过,不能让阴离子通过 |
某氢氧燃料电池的电解液是热的KOH溶液,在正极上氧气被还原,在负极上氢气被氧化,下列有关该电池的叙述正确的是
| A.负极反应式为:H2+2OH- -2e- =2H2O |
| B.正极反应式为:O2 +4H+十4e- =2H2O |
| C.工作一段时间后,KOH溶液的浓度不变 |
| D.电池工作时,电子由正极通过外电路流向负极 |
用质量均为100g的铜作电极,电解硝酸银溶液(足量),电解一段时间后,两电极的质量差为28g,此时两电极的质量分别为( )
| A.阳极100g,阴极128g | B.阳极93.6g,阴极121.6g |
| C.阳极91.0g,阴极119.0g | D.阳极86.0g,阴极114.0g |
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。下列有关氢氧燃料电池的说法不正确的是( )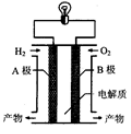
| A.A电极是负极 |
| B.外电路中电子由B电极通过导线流向A电极 |
| C.产物为无污染的水,属于环境友好电池 |
| D.该电池的总反应:2H2+O2===2H2O |
全钒流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置, 其原理如图所示,其中H+的作用是参与正极反应,并通过交换膜定向移动使右槽溶液保持电中性。下列有关说法不正确的是( )
| A.放电时当左槽溶液逐渐由黄变蓝,其电极反应式为:VO2+ +e一+2H+=VO2+ +H2O |
| B.充电时若转移的电子数为3.01×1023个,左槽溶液中n(H+)的变化量为l.0mol |
| C.充电时,H+由左槽定向移动到右槽 |
| D.充电过程中,右槽溶液颜色逐渐由绿色变为紫色 |
 从H+、K+、Cu2+、Cl-、SO中选取适当的离子组成符合下列情况的电解质。惰性电解,电 解质的物质的量减少,水的物质的量也减少,pH下降,则电解质的化学式为( )
从H+、K+、Cu2+、Cl-、SO中选取适当的离子组成符合下列情况的电解质。惰性电解,电 解质的物质的量减少,水的物质的量也减少,pH下降,则电解质的化学式为( )
| A.HCl | B.K2SO4 | C.CuSO4 | D.KCl |
 2CO2+4H2O。下列关于该电池的分析:①甲醇是负极②H+向负极移动③负极反应:CH3OH-6e-+H2O=CO2+6H+ ④1 mol CH3OH完全反应转移12 mol电子 ⑤正极反应:O2+4e-+2H2O==4OH-⑥该电池的电解质溶液可能是碱液。其中正确的是
2CO2+4H2O。下列关于该电池的分析:①甲醇是负极②H+向负极移动③负极反应:CH3OH-6e-+H2O=CO2+6H+ ④1 mol CH3OH完全反应转移12 mol电子 ⑤正极反应:O2+4e-+2H2O==4OH-⑥该电池的电解质溶液可能是碱液。其中正确的是