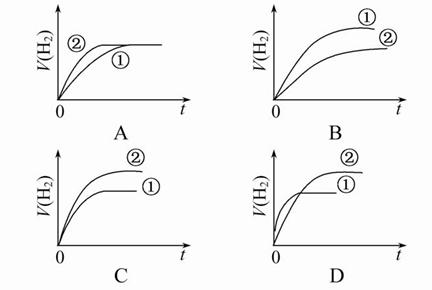
对室温下氢离子浓度、体积均相同的HCl溶液和CH3COOH溶液分别采取以下措施,有关叙述正确的是( )
| A.加适量的CH3COONa晶体,两溶液的氢离子浓度减小 |
| B.使温度升高20 ℃,两溶液的氢离子浓度不变 |
| C.加水稀释2倍,两溶液的氢离子浓度增大 |
| D.加足量的Zn充分反应后,两溶液中产生的氢气一样多 |
下列关于电解质溶液的叙述正确的是( )
A.常温下,由0.1 mol·L-1一元碱BOH溶液的pH=10,可推知BOH溶液存在:BOH B++OH- B++OH- |
| B.常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) |
| C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D.将pH=4的盐酸稀释后,溶液中所有离子的浓度均降低 |
已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10分别是三种酸的电离平衡常数,若已知这些酸可发生如下反应:
①NaCN+HNO2=HCN+NaNO2,
②NaCN+HF=HCN+NaF,
③NaNO2+HF=HNO2+NaF。
由此可判断下列叙述中,不正确的是( )
| A.HF的电离平衡常数为7.2×10-4 |
| B.HNO2的电离平衡常数为4.9×10-10 |
| C.根据①③两个反应即可知三种酸的相对强弱 |
| D.HNO2的电离平衡常数比HCN大,比HF小 |
0.1 mol·L-1氨水10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是( )
①电离程度增大;②c(NH3·H2O)增大;③NH4+数目增多;④c(OH-)增大;⑤导电性增强;⑥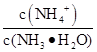 增大
增大
| A.①②③ | B.①③⑤ | C.①③⑥ | D.②④⑥ |
将浓度为0.1 mol·L-1 HF溶液加水不断稀释,下列各量始终保持增大的是( )
| A.c(H+) | B.Ka(HF) | C.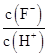 | D.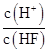 |
室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
| A.溶液中导电粒子的数目减少 |
B.溶液中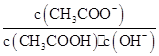 不变 不变 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
| D.再加入10 mL pH=11的NaOH溶液,混合液pH=7 |
甲酸的下列性质中,可以证明它是弱电解质的是( )
| A.1 mol / L甲酸溶液的c(H+)="0.01" mol/L |
| B.甲酸能与水以任何比例互溶 |
| C.10 mL 1 mol/L甲酸恰好与10 mL 1 mol/L NaOH溶液完全反应 |
| D.甲酸溶液的导电性比盐酸的弱 |
25 ℃时,在等体积的①pH=0的硫酸溶液、②0.05 mol/L的Ba(OH)2溶液、③pH=10的Na2S溶液、④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是( )
| A.1∶10∶1010∶109 | B.1∶5∶5×109∶5×108 |
| C.1∶20∶1010∶109 | D.1∶10∶104∶109 |