下列叙述正确的是( )
| A.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7 |
| B.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| C.常温下,向NH4Cl溶液中加入氨水至溶液的pH=7,此时溶液中c(NH4+)>c(C1-) |
| D.0.1mol·L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
下列各溶液的叙述中不正确的是( )
A.等pH的硫酸与醋酸稀释后pH的变化如图所示,则曲线Ⅱ表示的是醋酸的稀释图像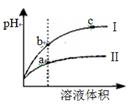 |
| B.溶有等物质的量的NaClO、NaHCO3的溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C.若NH4HCO3溶液、NH4HSO4溶液中c(NH4+)相等,则: c(NH4HSO4)<c(NH4HCO3) |
| D.已知某温度下Ksp(CH3COOAg) = 2.8×10-3,浓度均为0.1 mol·L-1的AgNO3溶液和CH3COONa溶液等体积混合一定能产生CH3COOAg沉淀 |
已知25℃,醋酸、次氯酸、碳酸、亚硫酸的电离平衡常数如表,下列叙述正确的是
| 酸 | 电离平衡常数 |
| 醋酸 | K i=1.75×10-5 |
| 次氯酸 | K i=2.98×10-8 |
| 碳酸 | Ki1=4.30×10-7 Ki2=5.61×10-11 |
| 亚硫酸 | Ki1=1.54×10-2 Ki2=1.02×10-7 |
A.25℃,等PH值的CH3COONa、NaClO、Na2CO3和Na2SO3四种溶液中,物质的量最小的是Na2CO3
B.少量的SO2通入NaClO溶液中反应的离子方程式为:SO2 + H2O + 2ClO—
 SO32— + 2HClO
SO32— + 2HClOC.少量CO2通入Ca(ClO)2溶液中反应的离子方程式为:CO2 + H2O + ClO—
 HCO3— + HClO
HCO3— + HClOD.向pH=a的醋酸溶液中加一定量水,所得溶液的pH>a、pH<a、pH=a均有可能
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知: pX=-lgc(X)。下列说法正确的是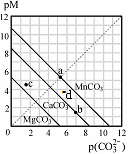
| A.在该温度下,MgCO3、MnCO3的溶解度依次增大 |
| B.d点可表示MnCO3的过饱和溶液,且c(Mn2+)>c(CO32-) |
| C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) |
| D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)>c(CO32-) |
给试管中某红色溶液加热,溶液颜色逐渐变浅,则原溶液可能是
①滴有石蕊的NH4Cl溶液 ②滴有酚酞的氨水溶液 ③滴有石蕊的H2SO4溶液 ④滴有酚酞的饱和氢氧化钙溶液 ⑤滴有酚酞的Na2CO3溶液 ⑥溶有SO2的品红溶液
| A.②④ | B.①③⑤ | C.①④⑥ | D.②③ |
已知25 ℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡 常数(25 ℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
由此可得出
A.对应钠盐溶液pH关系为: pH(Na2CO3) > pH(NaCN) > pH(CH3COONa)
B.CO2通入NaCN溶液中有:CO2+H2O+2NaCN→Na2CO3+2HCN
C.冰醋酸中逐滴加水,溶液的导电性、pH均先增大后减小
D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-) +2c(CO32-)
常温下向四份0.1 mol·L-1的醋酸钠溶液中分别加入少量冰醋酸、硫酸氢钠固体、醋酸钠固体、氢氧化钠固体(忽略溶液体积及温度变化),则溶液中c(Ac-)/c(Na+)变化正确的是
| A.增大、增大、不变、减小 |
| B.增大、减小、增大、减小 |
| C.减小、增大、增大、减小 |
| D.增大、减小、不变、减小 |
少量二氧化碳通入NaCN溶液中,发生如下反应:CO2 + H2O + CN- =HCO3- + HCN。以下说法正确的是(温度均为25℃)
| A.电离常数:K(HCN) <Ka2 (H2CO3) |
| B.浓度均为0.1mol·L-1的NaCN和NaHCO3溶液的pH:NaCN <NaHCO3 |
| C.浓度均为0.1mol·L-1的NaCN和Na2CO3溶液中,阴离子总浓度相等 |
| D.pH均为10的 Na2CO3溶液、NaCN溶液中,水电离产生的c(OH-)相等 |

 H+ + HA-;HA—
H+ + HA-;HA—  H+ + A2-
H+ + A2-