题目内容
给试管中某红色溶液加热,溶液颜色逐渐变浅,则原溶液可能是
①滴有石蕊的NH4Cl溶液 ②滴有酚酞的氨水溶液 ③滴有石蕊的H2SO4溶液 ④滴有酚酞的饱和氢氧化钙溶液 ⑤滴有酚酞的Na2CO3溶液 ⑥溶有SO2的品红溶液
| A.②④ | B.①③⑤ | C.①④⑥ | D.②③ |
A
解析试题分析:① NH4Cl是强酸弱碱盐,在溶液中NH4+水解是溶液呈酸性,所以滴加石蕊试液溶液变为红色。由于盐水解反应是吸热反应,所以升高温度,NH4Cl水解程度增大,溶液的酸性增强,溶液红色逐渐加深。错误。②氨水显碱性,滴加酚酞溶液变为红色。给试管加热,由于氨水不稳定,受热容易分解,氨气逸出,溶液的碱性减弱,所以红色变浅。正确。③H2SO4溶液是酸性的,能使紫色石蕊试液变为红色。由于它是强电解质,稳定性强。加热时既不分解,也不再电离,所以溶液的红色不变。错误。④氢氧化钙是强碱,能使无色的酚酞变为红色,但其溶解度随温度的升高而降低,所以给试管中的时饱和氢氧化钙溶液加热时由于溶解度的减小c(OH-)降低,溶液的碱性减弱,所以红色变浅。正确。⑤Na2CO3是强碱弱酸盐水解使溶液显碱性所以滴加酚酞试液变为红色。由于升高温度促进盐的水解,所以加热试管时红色变深。错误。⑥品红溶液是红色的,当其中溶有SO2的时候,由于SO2有漂白性,所以溶液呈无色。该无色物质不稳定,受热容易分解。所以给试管中的物质加热时溶液又变为红色。错误。
考点:考查物质的化学性质及相应的实验现象的知识。

 阅读快车系列答案
阅读快车系列答案关于室温下下列溶液的说法不正确的是
| A.水的电离程度:①=②=③=④ |
| B.分别加水稀释10倍,溶液的pH:①>②>③>④ |
C.①、③两溶液等体积混合: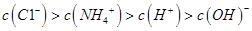 |
D.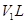 溶液②与 溶液②与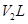 溶液③混合,若 溶液③混合,若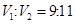 ,则混合溶液pH=4(忽略溶液体积变化) ,则混合溶液pH=4(忽略溶液体积变化) |
将氯化铝溶液蒸干并灼烧后得到纯净的固体A,将A在高温下熔融后用铂电极进行电解,下列有关电极产物的判断正确的是
| A.阴极产物是氢气 | B.阳极产物是氧气 |
| C.阴极产物是铝和氧气 | D.阳极产物只有氯气 |
下列叙述正确的是( )
| A.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7 |
| B.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| C.常温下,向NH4Cl溶液中加入氨水至溶液的pH=7,此时溶液中c(NH4+)>c(C1-) |
| D.0.1mol·L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
下列溶液在空气中加热、蒸干、灼烧后,所得固体为原溶液中的溶质的是( )
| A.NaHCO3 | B.KMnO4 | C.FeCl3 | D.NaCl |
下列关于电离常数的说法正确的是( )
| A.电离常数随着弱电解质的浓度增大而增大 |
| B.CH3COOH的电离常数表达式为Ka= |
| C.CH3COOH溶液中加入少量CH3COONa溶液,电离常数减小 |
| D.电离常数只与温度有关,与浓度无关 |
下列叙述正确的是 ( )
| A.一般认为沉淀离子浓度小于10-4 mol/L时,则认为已经沉淀完全 |
| B.反应AgCl+NaBr=AgBr+NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水 |
C.Al(OH)3(s) Al3+(aq)+3OH-(aq)表示沉淀溶解平衡,Al(OH)3 Al3+(aq)+3OH-(aq)表示沉淀溶解平衡,Al(OH)3 Al3++3OH-表示水解平衡 Al3++3OH-表示水解平衡 |
| D.只有反应速率很高的化学反应才能应用于工业生产 |
已知相同条件下,HClO的电离常数小于H2CO3的一级电离常数(Ka)。为了提高氯水中HClO的浓度,可加入( )
| A.NaCl(s) | B.CaCO3(s) | C.H2O | D.NaOH(s) |
把1 L 0.1 mol/L醋酸溶液用蒸馏水稀释到10 L,下列叙述正确的是 ( )
| A.c(CH3COOH)变为原来的1/10 |
| B.c(H+)变为原来的1/10 |
| C.c(CH3COO-)/c(CH3COOH)的比值增大 |
| D.溶液的导电性增强 |