常温下,在10 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入0.1 mol·L-1 HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是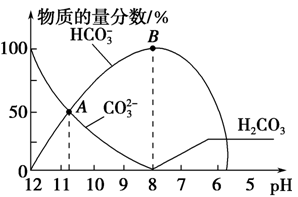
| A.在0.1 mol·L-1 Na2CO3溶液中:c(Na+)+ c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| B.当溶液的pH为7时,溶液的总体积为20 ml |
| C.在B点所示的溶液中,浓度最大的阳离子是Na+ |
| D.在A点所示的溶液中:c(CO32-)=c(HCO3-)>c(H+)>c(OH-) |
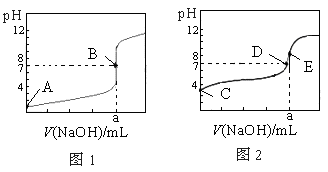
已知水在25℃和95℃时,其电离平衡曲线如图所示,下列说法错误的
| A.A曲线代表25℃时水的电离平衡曲线 |
| B.当95℃时,pH=6的溶液呈中性 |
| C.25℃时,将10mLpH=12的NaOH溶液与1mLpH=1的H2SO4 溶液混合,所得溶液的pH=7 |
| D.95℃时,等体积等物质的量浓度的HA溶液和NaOH溶液混合后,当混合溶液的pH=6时,说明HA酸为弱酸 |
有①Na2CO3溶液 ②CH3COONa溶液 ③NaOH溶液各25mL,物质的量浓度均为0.1 mol/L,下列说法正确的是( )
| A.3种溶液pH的大小顺序是③>②>① |
| B.若将3种溶液稀释相同倍数,pH变化最大的是② |
| C.若分别加入25mL0.lmol/L盐酸后,pH最大的是① |
| D.若用Pt电极电解3种溶液一段时间后,pH均不变 |
室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法错误的是( )
| A.溶液中导电粒子的数目增加 |
B.溶液中 不变 不变 |
| C.醋酸的电离程度增大,但电离平衡常数Ka不变 |
| D.再加入10 mL pH=11的NaOH溶液,恰好完全中和 |
在蒸发皿中加热蒸干再加热(低于400℃)下列物质的溶液,可以得到该物质固体的是( )
| A.氯化铝 | B.碳酸氢钠 | C.硫酸亚铁 | D.硫酸镁 |
下列物质中,属于弱电解质的是( )
| A.氨水 | B.冰醋酸 | C.酒精 | D.硫酸钡 |
有关AgCl的沉淀溶解平衡的说法正确的是
| A.AgCl沉淀生成和溶解同时在不断进行,且速率相等 |
| B.AgCl难溶于水,溶液中没有Ag+和Cl- |
| C.用等体积的蒸馏水和0.01mol·L-1的盐酸洗涤AgCl沉淀,用水洗涤造成的AgCl的损失小于用稀盐酸洗涤的损失量。 |
| D.向含有AgCl的悬浊液中加入NaBr固体,AgCl沉淀不变化 |
下列叙述不正确的是
| A.CaCO3能够溶解在CO2的水溶液中 |
| B.Mg(OH)2可溶于盐酸,不溶于NH4Cl溶液 |
| C.AgCl可溶于氨水 |
| D.MgSO4溶液中滴加Ba(OH)2得到两种沉淀 |